Ultimo aggiornamento 23/07/2023
Il tamoxifene (C26H29NO) è un farmaco che appartiene alla classe degli antiestrogeni non steroidei; è un derivato del trifeniletilene, 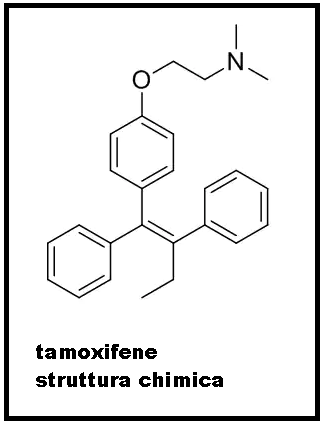 precursore anche del più utilizzato clomifene citrato.
precursore anche del più utilizzato clomifene citrato.
Introdotto in commercio negli anni ’90, rappresenta ancora oggi il cardine della terapia endocrinologica del carcinoma della mammella femminile e maschile sia dopo l’intervento chirurgico di prima istanza, sia dopo l’eventuale recidive, in caso di positività recettoriale.
La terapia con TMX determina un miglioramento assoluto del 9% in termini di sopravvivenza a 10 anni nelle pazienti con cancro mammario. E’ inoltre utilizzato per la prevenzione del cancro mammario controlaterale (riduzione del 50% del rischio).
Il tamoxifene (Nolvadex® cpr 10 mg, 20 mg), agisce con meccanismo di competizione recettoriale con gli estrogeni (SERM):
1. occupando il sito  recettoriale estrogenico ipofisario impedisce l’effetto feed-back negativo degli estrogeni sulla secrezione gonadotropinica.
recettoriale estrogenico ipofisario impedisce l’effetto feed-back negativo degli estrogeni sulla secrezione gonadotropinica.
2. legandosi ai recettori estrogenici nei tumori ER-positivi svolge un’efficace azione antineoplastica.
Il TMX è commercializzato in Italia con il nome di Nolvadex® che si presenta in forma di compresse da 10 e 20 mg. La posologia post-chirurgica del cancro mammario è di 20 mg/die, da assumersi preferibilmente sempre alla stessa ora; viene assorbito a livello intestinale e viaggia in circolo legato all’albumina plasmatica per raggiungere gli organi target.
Giacché il tamoxifene può causare senso di nausea e lasciare un sapore metallico in bocca, alcune pazienti preferiscono prenderlo durante i pasti. Normalmente il trattamento con il tamoxifene è prescritto per cinque anni, anche se alcuni oncologi lo prescrivono per due anni e altri a tempo indeterminato. Attualmente si ritiene che cinque anni siano la durata ideale per le pazienti in pre-menopausa, mentre per le pazienti in post-menopausa la durata è variabile.
EFFETTI COLLATERALI
- SINDROME PRE-MENOPAUSALE. Vampate di calore, sudorazioni notturne, perdite vaginali, secchezza e prurito vaginale, riduzione del desiderio sessuale e dispareunia sono comuni durante il trattamento. I sintomi tendono ad essere più accentuati nelle pazienti in premenopausa e nelle donne in post-menopausa precedentemente trattate con terapia ormonale sostitutiva. I disturbi vasomotori divengono meno pronunciati dopo alcuni mesi di terapia e tendono a scomparire gradualmente col tempo, ma non per tutte le pazienti. Può giovare ridurre il consumo di tè, caffè, tabacco e alcool anche se alcuni studi confermano l’effetto adiuvante del caffè nel potenziamento dell’efficacia del TMX. Anche la somministrazione di progesterone e alcuni farmaci antidepressivi può essere efficace nel lenire i disturbi vasomotori.
- Nausea e indigestione. Sono abbastanza frequenti all’inizio del trattamento, ma tendono a scomparire dopo le prime settimane. La nausea scompare spesso spontaneamente, ma se persiste può essere trattata con efficacia con i farmaci antiemetici. Può giovare assumere le compresse a stomaco pieno o con il latte.
- Aumento dell’appetito. È l’effetto collaterale più comune. Un regime dietetico adeguato può servire a limitarne le conseguenze.
- Modificazioni del ciclo mestruale. Le donne che non sono ancora in età menopausale potrebbero notare che il ciclo mestruale si modifica: le mestruazioni diventano irregolari, scarse o talvolta addirittura scompaiono.
- Depressione, stanchezza e vertigini. Alcune pazienti si sentono depresse durante il trattamento con tamoxifene, ma ciò può dipendere da altre cause.
- Cefalea. Alcune pazienti sofferenti di emicrania hanno descritto un aumento del disturbo. Può giovare bere molto,
- Trombosi venose superficiali e profonde e trombosi polmonari. Compaiono dolore, sensazione di calore, gonfiore o sensibilità localizzati a un arto, oppure dolore toracico.
- Trombocitopenia (generalmente limitata a valori compresi tra 80.000 e 90.000/mmc, senza conseguenze emorragiche) e leucopenia. Raramente tali fenomeni sono di gravità tale da provocare la sospensione della terapia. Si consiglia comunque un controllo dell’emocromo e delle piastrine dopo 15-20 giorni dall’inizio del trattamento e, successivamente, ogni 6 mesi.
- Disturbi della vista. Opacità subcapsulari posteriori del cristallino (cataratta) sono le patologie oculari più comuni. Riportati casi di retinopatia utilizzando dosi elevate di TMX, non confermati però da studi condotti utilizzando dosi standard del farmaco.
- Modificazioni della voce. Sono state riferite da alcune pazienti, e chi è cantante di professione potrebbe richiedere una consulenza specifica.
iPERPLASIA E CARCINOMA DELL’ENDOMETRIO: è il più temuto fra gli effetti collaterali del TMX.
Il TMX benchè agisca come antagonista estrogenico sulla mammella, su altri organi estrogeni positivi, come l’endometrio, agisce come agonista. Alcuni studi hanno dimostrato che le pazienti che assumono tamoxifene in dosi elevate per un lungo periodo hanno un rischio leggermente accresciuto di sviluppare ispessimento dell’endometrio >5 mm, iperplasia endometriale con atipie, polipi endometriali, endometriosi e leiomiomi.
Siccome anche le cellule stromali contengono recettori per gli estrogeni, possono insorgere anche sarcomi e tumori mesodermici misti maligni dell’utero.
Le pazienti in terapia con TMX più facilmente vanno incontro a curettage, isterectomia e annessiectomia bilaterale.
Solamente tra le donne in premenopausa si è avuto un rischio significativamente aumentato di cisti ovariche. Tuttavia, questi rischi devono essere valutati rispetto ai benefici derivanti dal trattamento, che per la maggior parte delle pazienti sono di gran lunga superiori ai rischi.
SCREENING DI CONTROLLO: si effettua ogni 6 mesi e/o in caso di sanguinamento uterino anomalo (AUB) e si avvale dell’ecografia transvaginale e dell’isteroscopia; in alcuni casi può essere utile l’isterosonografia e una biopsia endometriale.
Ecografia transvaginale:
è l’esame di prima scelta per il follow-up della terapia con TMX. La vicinanza del trasduttore all’utero e l’assenza dell’interposizione della vescica, permette una valutazione ottimale dell’endometrio. Lo spessore dell’endometrio normale non supera i 5 mm. Numerosi studi hanno confermato che le patologie endometriali, surriferite, sono presenti nel 60% delle pazienti in cui lo spessore dell’endometrio supera il cut-off di 8 mm mentre nel gruppo con endometrio di spessore <6 mm le patologie endometriali sono presenti solo nel 6.2%.
Isteroscopia:
L’ISC è l’esame diagnostico di IIa scelta a cui si accede se l’ETV evidenzia una patologia endocavitaria (ispessimento endometrio, polipi, miomi). L’ISC oltre a confermare la diagnosi ecografica, permette anche di effettuare una biopsia e/o l’eliminazione della lesione. Il timore di diffusione di cellule neoplastiche in cavità peritoneale non deve essere un fattore di impedimento per l’esame isteroscopico.
La valutazione isteroscopica della cavità uterina prima dell’inizio della somministrazione di tamoxifene, può aiutare ad identificare le pazienti ad alto rischio di lesioni, dunque più sensibili agli effetti cancerogeni del tamoxifene. D’altra parte, il tasso molto basso di lesioni atipiche emergenti associate all’assunzione di tamoxifene suggerirebbe l’ipotesi che il tamoxifene agisca da promotore, e non come causa diretta, di lesioni già esistenti.
Isterosonografia: mostra una sensibilità dell’87% ed una specificità del 100% nel valutare l’iperplasia endometriale
Teratogenicità del TMX. Le pazienti devono evitare gravidanze prima di 6 mesi dalla sospensione della terapia con TMX.
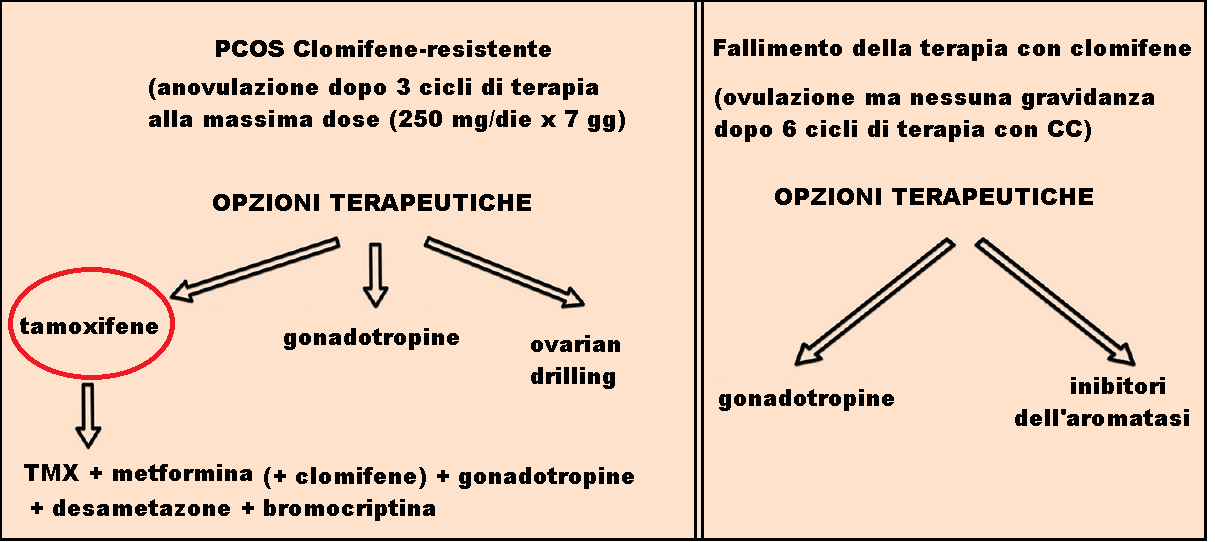
TMX e induzione dell’ovulazione in pazienti PCOS – il TMX potrebbe essere utilizzato, come alternativa o in associazione al Clomifene, per indurre ovulazione nelle pazienti PCOS anovulatorie resistenti al clomifene (127,128). Induce un’aumentata secrezione di gonadotropine ma presenta un importante effetto antiestrogenico perfiferico.
Bibliografia:
- C. K. Osborn: “Tamoxifen in the Treatment of Breast Cancer”, N Engl J Med 1998, 339: 1609-18
- H.J. Burstein et al.: “Primary Care for Survivors of Breast Cancer”, N Engl J Med 2000, 343: 1086-94.
- M. Clemons et al.: “Estrogen and the Risk of Breast Cancer”, N Engl J Med 2001, 344: 276-85.
- Marchesoni D, Driul L, Fabiani G,Di Loreto C, Cataldi P, Mozzanega B. Endometrial histologic changes in post-menopausal breast cancer patients using tamoxifen. International Journal of Gynecology & Obstetrics 2001; 7: 257-262.
- Jaiyesimi IA, Buzdar AU, Decker DA, Hortobagyi GN “Use of tamoxifen for breast cancer: twenty-eight years later.” J Clin Oncol 13 (1995): 513-29
- Ellis PM, Tattersall MHN “Tamoxifen flare – an unusual case of hypercalcaemia and transient rapidly progressive pancytopenia.” Aust N Z J Med 25 (1995): 375-6
- “Product Information. Nolvadex (tamoxifen).” Zeneca Pharmaceuticals, Wilmington, DE.
- Andersson M, Storm HH, Mouridsen HT “Carcinogenic effects of adjuvant tamoxifen treatment and radiotherapy for early breast cancer.” Acta Oncol 31 (1992): 259-63
- Friedl A, Jordan VC “What do we know and what don’t we know about tamoxifen in the human uterus.” Breast Cancer Res Treat 31 (1994): 27-39
- Cohen I, Shapira J, Altaras M, Cordoba M, Rosen D, Beyth Y “Endometrial decidual changes in a postmenopausal woman treated with tamoxifen and megestrol acetate.” Br J Obstet Gynaecol 99 (1992): 773-4
- Fisher B, Costantino JP, Redmond CK, Fisher ER, Wickerham DL, Cronin WM, Bowman D, Couture J, Dimitrov NV, Evans J, Farrar “Endometrial cancer in tamoxifen-treated breast cancer patients – findings from the national surgical adjuvant breast and bowel project (NSABP) b-14.” J Natl Cancer Inst 86 (1994): 527-37
- Seoud MA, Johnson J, Weed JC “Gynecologic tumors in tamoxifen-treated women with breast cancer.” Obstet Gynecol 82 (1993): 165-9
- Dilts PV, Jr Hopkins MP, Chang AE, Cody RL “Rapid growth of leiomyoma in patient receiving tamoxifen.” Am J Obstet Gynecol 166 (1992): 167-8
- Timmerman D, Vergote I “Tamoxifen-induced endometrial polyp.” N Engl J Med 335 (1996): 1650
- Jordan VC, Morrow M “Should clinicians be concerned about the carcinogenic potential of tamoxifen?” Eur J Cancer 30A (1994): 1714-21
- Ugwumadu AH, Bower D, Ho PK “Tamoxifen induced adenomyosis and adenomyomatous endometrial polyp.” Br J Obstet Gynaecol 100 (1993): 386-8
- Stewart HJ “The Scottish trial of adjuvant tamoxifen in node-negative breast cancer.” Natl Cancer Inst Monogr 11 (1992): 117-20
- Fornander T, Cedermark B, Mattsson A, et al. “Adjuvant tamoxifen in early breast cancer: occurrence of new primary cancers.” Lancet 21 (1989): 117-20
- Gal D, Kopel S, Bashevkin M, Lebowicz J, Lev R, Tancer ML “Oncogenic potential of tamoxifen on endometria of postmenopausal women with breast cancer–preliminary report.” Gynecol Oncol 42 (1991): 120-3
- Van Leeuwen FE, Benraadt J, Coebergh JW, et al. “Risk of endometrial cancer after tamoxifen treatment of breast cancer.” Lancet 343 (1994): 448-52
- Mack T “Tamoxifen ruling in California.” Science 270 (1995): 1102-3
- Ismail SM “Pathology of endometrium treated with tamoxifen.” J Clin Pathol 47 (1994): 827-33
- Ismail SM “The effects of tamoxifen on the uterus.” Curr Opin Obstet Gynecol 8 (1996): 27-31
- Wysowski DK, Honig SF, Beitz J “Uterine sarcoma associated with tamoxifen use.” N Engl J Med 346 (2002): 1832-3
- Committee on Gynecologic Practice “Tamoxifen and endometrial cancer.” Int J Gynaecol Obstet 53 (1996): 197-9
- fornander T, Hellstrom AC, Moberger B “Descriptive clinicopathologic study of 17 patients with endometrial cancer during or after adjuvant tamoxifen in early breast cancer.” J Natl Cancer Inst 85 (1993): 1850-5
- Mccluggage WG, Varma M, Weir P, Bharucha H “Uterine leiomyosarcoma in patient receiving tamoxifen therapy.” Acta Obstet Gynecol Scand 75 (1996): 593-5
- Ribeiro G, Swindell R “The Christie Hospital adjuvant tamoxifen trial.” Natl Cancer Inst Monogr 11 (1992): 121-5
- Kang J, Baxi L, Heller D “Tamoxifen-induced growth of leiomyomas: a case report.” J Reprod Med 41 (1996): 119-20
- Barakat RR “Tamoxifen and endometrial neoplasia.” Clin Obstet Gynecol 39 (1996): 629-40
- Magriples U, Naftolin F, Schwartz PE, Carcangiu ML “High-grade endometrial carcinoma in tamoxifen-treated breast cancer patients.” J Clin Oncol 11 (1993): 485-90
- Wickerham DL, Fisher B, Wolmark N, et al. “Association of Tamoxifen and Uterine Sarcoma.” J Clin Oncol 20 (2002): 2758-2760
- Cross SS, Ismail SM “Endometrial hyperplasia in an oophorectomized woman receiving tamoxifen therapy. Case report.” Br J Obstet Gynaecol 97 (1990): 190-2
- Neven P, Demuylder X, Vanbelle Y, Campo R, Vanderick G “Tamoxifen and the uterus.” BMJ 309 (1994): 1313-4
- Coleman MP “Safety of tamoxifen.” Lancet 347 (1996): 836-7
- Gallo MA, Kaufman D. Antagonistic and agonistic effects of tamoxifen: significance in humancancer. Seminars in Oncology 1997; 24: 71–80.
- Corley D, Rowe J, Curtis MT, Hogan WM, Noumoff JS, Livolsi VA “Postmenopausal bleeding from unusual endometrial polyps in women on chronic tamoxifen therapy.” Obstet Gynecol 79 (1992): 111-6
- Divers MJ “Massive endometrial polyp after tamoxifen therapy.” Br J Clin Pract 49 (1995): 275-6
- Cuenca RE, Giachino J, Arrendondo MA, Hempling R, Edge SB “Endometrial carcinoma associated with breast carcinoma: low incidence with tamoxifen use.” Cancer 77 (1996): 2058-63
- Ford MR, Turner MJ, Wood C, Soutter WP “Endometriosis developing during tamoxifen therapy.” Am J Obstet Gynecol 158 (1988): 1119
- Rose PG, Alvarez B, MacLennan GT “Exacerbation of endometriosis as a result of premenopausal tamoxifen exposure.” Am J Obstet Gynecol 183 (2000): 507-8
- Glass AR “Paradoxical suppression of spermatogenesis during tamoxifen treatment of oligospermia.” Fertil Steril 49 (1988): 376-7
- Sobel JD, Chaim W, Leaman D “Recurrent vulvovaginal candidiasis associated with long-term tamoxifen treatment in postmenopausal women.” Obstet Gynecol 88 (suppl (1996): 704-6
- Court C “International group evaluates tamoxifen risks for women.” BMJ 312 (1996): 529
- “Tamoxifen under scrutiny as carcinogen in California.” Eur J Cancer 32A (1996): 567
- Thylan S “Tamoxifen-associated ovarian cysts may be endometriomas.” Am J Obstet Gynecol 175 (1996): 752
- Neven P “Endometrial changes in patients on tamoxifen.” Lancet 346 (1995): 1292
- Sasco AJ “Tamoxifen and menopausal status: risks and benefits.” Lancet 347 (1996): 761
- Fisher B “Commentary on endometrial cancer deaths in tamoxifen-treated breast cancer patients.” J Clin Oncol 14 (1996): 1027-39
- Mcgonigle KF, Lantry SA, Odommaryon TL, Chai A, Vasilev SA, Simpson JF “Histopathologic effects of tamoxifen on the uterine epithelium of breast cancer patients: analysis by menopausal status.” Cancer Lett 101 (1996): 59-66
- Fernando IN, Tobias JS “Priapism in patient on tamoxifen .” Lancet 1 (1989): 436
- Cecchini S, Ciatto S, Bonardi R, Mazzotta A, Grazzini G, Pacini P, Muraca MG “Screening by ultrasonography for endometrial carcinoma in postmenopausal breast cancer patients under adjuvant tamoxifen.” Gynecol Oncol 60 (1996): 409-11
- Nasri MN, Shepherd JH, Setchell ME, Lowe DG, Chard T. Sonographic depiction of postmenopausal endometrium with transabdominal and transvaginal scanning. Ultrasound Obstet Gynecol. 1991 Jul 1;1(4):279-83.
- Lahti E, Blanco G, Kauppila A, Apaja-Sarkkinen M, Taskinen PJ, Laatikainen T. Endometrial changes in postmenopausal breast cancer patients receiving tamoxifen. Obstetrics and Gynecology 1993; 81: 660-664.
- Beşe T, Kösebay D, Demirkiran F, Arvas M, Beşe N, Mandel N. Ultrasonographic appearance of endometrium in postmenopausal breast cancer patients receiving tamoxifen. European Journal of Obstetrics & Gynecology and Reproductive Biology 1996; 67: 157-162.
- Garuti G. Cellani F, Centinaio G, Sita G, Nalli G, Luerti M. Baseline endometrial assessment before tamoxifen for breast cancer in asymptomatic menopausal women. Gynecologic Oncology 2005; 98: 63 – 67.
- Paschopoulos M, Kontostolis E, Lolis ED, Koliopoulos G, Alamanos Y, Paraskevaidis E. The Use of Transvaginal Sonography and Vaginoscopic Hysteroscopy in Women on Tamoxifen. Journal of the Society of Laparoendoscopic Surgeons 2001; 5: 211-214.
- . Khan F, Jamaat S, Al-Jaroudi D. Saline infusion sonohysterography versus hysteroscopy foruterine cavity evaluation. Annals of Saudi Medicine 2011; 31: 387-92.
- Diagnostic accuracy of sonohysterography, transvaginal sonography, and hysterosalpingography in patients with uterine cavity diseases. Soares SR, Barbosa dos Reis MM, Camargos AF. Fertil Steril. 2000 Feb; 73(2):406-11.
- Bianco AR. The ATAC („Arimidex‟, Tamoxifen, Alone or in Combination) adjuvant breast cancer trial: baseline endometrial sub-protocol data on the effectiveness of transvaginal ultrasonography and diagnostic hysteroscopy.Human Reproduction 2005; 20(1) : 294–301.
- Giorda G, Crivellari D, Veronesi A, Perin T, Campagnutta E, Carbone A, Scarabelli C. Comparison of ultrasonography, hysteroscopy,and biopsy in the diagnosis of endometrial lesions in postmenopausal tamoxifen-treated patients. Acta Obstetricia et Gynecologica Scandinavica 2002:81: 975–980.
- Timmerman D; Deprest I; Bourne T, Van den Berghe I, Collins WP, Vergote I.: A randomized trial on the use of ultrasonography or office hysteroscopy for endometrial assessment in postmenopausal patients with breast cancer who were treated with tamoxifen. The American Journal of Obstetrics and Gynecology 1998 179: 62-70.
- De Kroon CD, Hiemstra E, Trimbos JB, Jansen FW. Power Doppler area in the diagnosis ofendometrial cancer. International Journal of Gynecological Cancer 2010; 20: 1160-5.
- Dijkhuizen FP, De Vries LD, Mol BW, Brölmann HA, Peters HM, Moret E, Heintz AP. Comparison of transvaginal ultrasonography and saline infusion sonography for the detection of intracavitary abnormalities in premenopausal women. Ultrasound in Obstetrics and Gynecology 2000; 15: 372-6.
- Garuti G, Cellani F, Grossi F, Colonnelli M, Centinaio G, Luerti M. Saline Infusion Sonography and Office Hysteroscopy to Assess Endometrial Morbidity Associated with Tamoxifen Intake. Gynecologic Oncology 2002; 86, 323–329.
- Bingol B, Gunenc MZ, Gedikbasi A, Guner H, Tasdemir S, Tiras B. Comparison of diagnostic accuracy of saline infusion sonohysterography, transvaginal sonography and hysteroscopy in postmenopausal bleeding. Archives of Gynecology and Obstetrics 2011;284:111-7.
- Marconi D, Exacoustos C, Cangi B, Perroni A, Zupi E, Valli E, Romanini C. Transvaginal sonographic and hysteroscopic findings in postmenopausal women receiving tamoxifen. The Journal of the American Association of Gynecologic Laparoscopists 1997 4(3): 331-9.
- Franchi M, Ghezzi F, Donadello M, Zanaboni F, Beretta P, Bolis P. Endometrial Thickness in Tamoxifen-Treated Patients: An Independent Predictor of Endometrial Disease. Obstetrics and Gynecology 1999; 93: 1004–8.
- Clark TJ, Mann CH, Shah N, Khan KS, Song F, GuptaJK.: Accuracy of outpatient endometrial biopsy in the diagnosis of endometrial hyperplasia. Acta Obstetricia and Gynecologica Scandinavia 2001; 80: 784-93.
- Tinelli R, Tinelli FG, Cicinelli E, Malvasi A, Tinelli A. The role of hysteroscopy with eye-directed biopsy in postmenopausal women with uterine bleeding and endometrial atrophy. Menopause 2008; 15: 737-42.
- Zhu HL, Liang XD, Wang JL, Cui H, Wei LH. Hysteroscopy and directed biopsy in the diagnosis of endometrial carcinoma. Chinese Medical Journal 2010; 123: 3524-8.
- Polyzos NP, Mauri D, Tsioras S, Messini CI, Valachis A, Messinis IE Intraperitoneal dissemination of endometrial cancer cells after hysteroscopy: a systematic review and meta-analysis. International Journal of Gynecological Cancer 2010; 20: 261-7.
- Shushan A, Peretz T, Uziely B, Lewin A, Moryosef S “Ovarian cysts in premenopausal and postmenopausal tamoxifen-treated women with breast cancer.” Am J Obstet Gynecol 174 (1996): 141-4
- Agrawal BL, Zelkowitz L “Bone ‘flare,’ hypercalcemia, and jaundice after tamoxifen therapy .” Arch Intern Med 141 (1981): 1240
- Creamer P, Lim K, George E, Dieppe P “Acute inflammatory polyarthritis in association with tamoxifen.” Br J Rheumatol 33 (1994): 583-5
- Kenny AM, Prestwood KM, Pilbeam CC, Raisz LG “The short term effects of tamoxifen on bone turnover in older women.” J Clin Endocrinol Metab 80 (1995): 3287-91
- Noguchi M, Taniya T, Tajiri K, Miwa K, Miyazaki I, Koshino H, Mabuchi H, Nonomura A “Fatal hyperlipaemia in a case of metastatic breast cancer treated by tamoxifen.” Br J Surg 74 (1987): 586-7
- Love RR, Bardon HS, Mazess RB, Epstein S, Chappell RJ “Effect of tamoxifen on lumbar spine bone mineral density in postmenopausal women after 5 years.” Arch Intern Med 154 (1994): 2585-8
- Fentiman IS, Caleffi M, Rodin A, Murby B, Fogelman I “Bone mineral content of women receiving tamoxifen for mastalgia.” Br J Cancer 60 (1989): 262-4
- Gibson TC “Severe hypercalcaemia and tamoxifen ‘flare’.” Br J Clin Pract 44 (1990): 716-7
- Larsen W, Fellowes G, Rickman LS “Life-threatening hypercalcemia and tamoxifen.” Am J Med 88 (1990): 440-2
- Kalef-Ezra J, Glaros D, Klouvas G, Hatzikonstantinou J, Karantanas A, Siamopoulos KC, Pavlidis N “New evidence that tamoxifen does not induce osteoporosis: a nuclear activation analysis and absorptiometry study.” Br J Radiol 65 (1992): 417-20
- Neal AJ, Evans K, Hoskin PJ “Do long-term administration of tamoxifen affect bone mineral density.” Eur J Cancer 29A (1993): 1971-3
- Bruning PF, Bonfrer JM, Hart AA, de Jong-Bakker M, Linders D, van Loon J, Nooyen WJ “Tamoxifen, serum lipoproteins and cardiovascular risk.” Br J Cancer 58 (1988): 497-9
- Love RR, Mazess RB, Epstein S, Wiebe DA, Demets DL “Bone mineral density (BMD) preservation with tamoxifen treatment in postmenopausal women: results of a placebo-controlled trial (MEETING ABSTRACT).” Breast Cancer Res Treat 16 (1990): 145
- Blackburn AM, Amiel SA, Millis RR, Rubens RD “Tamoxifen and liver damage.” Br Med J (Clin Res Ed) 289 (1984): 288
- Van Hoof M, Rahier J, Horsmans Y “Tamoxifen-induced steatohepatitis.” Ann Intern Med 124 (1996): 855-6
- Pratt DS, Knox TA, Erban J “Tamoxifen-induced steatohepatitis.” Ann Intern Med 123 (1995): 236
- Ching CK, Smith PG, Long RG “Tamoxifen-associated hepatocellular damage and agranulocytosis .” Lancet 339 (1992): 940
- Pinto HC, Baptista A, Camilo ME, Decosta EB, Valente A, Demoura MC “Tamoxifen-associated steatohepatitis – report of three cases.” J Hepatol 23 (1995): 95-7
- Loomus GN, Aneja P, Bota RA “A case of peliosis hepatis in association with tamoxifen therapy.” Am J Clin Pathol 80 (1983): 881-3
- Love RR, Surawicz TS, Williams EC “Antithrombin III level, fibrinogen level, and platelet count changes with adjuvant tamoxifen therapy.” Arch Intern Med 152 (1992): 317-20
- Mike V, Currie VE, Gee TS “Fatal neutropenia associated with long-term tamoxifen therapy.” Lancet 344 (1994): 541-2
- Pavlidis NA, Petris C, Briassoulis E, Klouvas G, Psilas C, Rempapis J, Petroutsos G “Clear evidence that long-term, low-dose tamoxifen treatment can induce ocular toxicity. A prospective study of 63 patients.” Cancer 69 (1992): 2961-4
- Zinchuk O, Watanabe M, Hayashi N, Fukushima A, Ueno H “A case of tamoxifen keratopathy.” Arch Ophthalmol 124 (2006): 1046-8
- Bentley CR, Davies G, Aclimandos WA “Tamoxifen retinopathy: a rare but serious complication.” BMJ 304 (1992): 495-6
- Griffiths MF “Tamoxifen retinopathy at low dosage.” Am J Ophthalmol 104 (1987): 185-6
- Mihm LM, Barton TL “Tamoxifen-induced ocular toxicity.” Ann Pharmacother 28 (1994): 740-2
- Heier JS, Dragoo RA, Enzenauer RW, Waterhouse WJ “Screening for ocular toxicity in asymptomatic patients treated with tamoxifen.” Am J Ophthalmol 117 (1994): 772-5
- Pugesgaard T, Von Eyben FE “Bilateral optic neuritis evolved during tamoxifen treatment.” Cancer 58 (1986): 383-6
- Morales M, Santana N, Soria A, Mosquera A, Ordovas J, Novoa J, Betancor P, Valeron PF, Diazchico B, Chirino R “Effects of tamoxifen on serum lipid and apolipoprotein levels in postmenopausal patients with breast cancer.” Breast Cancer Res Treat 40 (1996): 265-70
- Love RR, Cameron L, Connell BL, Leventhal H “Symptoms associated with tamoxifen treatment in postmenopausal women.” Arch Intern Med 151 (1991): 1842-7
- Mcdonald CC, Alexander FE, Whyte BW, Forrest AP, Stewart HJ “Cardiac and vascular morbidity in women receiving adjuvant tamoxifen for breast cancer in a randomised trial.” BMJ 311 (1995): 977-80
- Hendrick A, Subramanian VP “Tamoxifen and thromboembolism.” JAMA 243 (1980): 514-5
- Duggan C, Marriott K, Edwards R, Cuzick J “Inherited and acquired risk factors for venous thromboembolic disease among women taking tamoxifen to prevent breast cancer.” J Clin Oncol 21 (2003): 3588-93
- Love RR, Wiebe DA, Feyzi JM, Newcomb PA, Chappell RJ “Effects of tamoxifen on cardiovascular risk factors in postmenopausal women after 5 years of treatment.” J Natl Cancer Inst 86 (1994): 1534-9
- Jones AL, Powles TJ, Treleaven JG, Burman JF, Nicolson MC, Chung HI, Ashley SE “Haemostatic changes and thromboembolic risk during tamoxifen therapy in normal women.” Br J Cancer 66 (1992): 744-7
- Smith RP, Dewar JA, Winter JH “Tamoxifen-induced asthma .” Lancet 341 (1993): 772
- Masala A, Delitala G, Lo Dico G, Stoppelli I, Alagna S, Devilla L “Inhibition of lactation and inhibition of prolactin release after mechanical breast stimulation in puerperal women given tamoxifen or placebo.” Br J Obstet Gynaecol 85 (1978): 134-7
- Anelli TFM, Anelli A, Tran KN, Lebwohl DE, Borgen PI “Tamoxifen administration is associated with a high rate of treatment- limiting symptoms in male breast cancer patients.” Cancer 74 (1994): 74-7
- Gordon D, Beastall GH, McArdle CS, Thomson JA “The effect of tamoxifen therapy on thyroid function tests.” Cancer 58 (1986): 1422-5
- Ron IG, Inbar MJ, Barak Y, Stier S, Chaitchik S “Organic delusional syndrome associated with tamoxifen treatment.” Cancer 69 (1992): 1415-7
- Drago F, Arditi M, Rebora A “Tamoxifen and purpuric vasculitis .” Ann Intern Med 112 (1990): 965-6
- Parry BR “Radiation recall induced by tamoxifen .” Lancet 340 (1992): 49
- Lopez M, Lelliott CJ, Tovar S, et al. “Tamoxifen-Induced Anorexia Is Associated With Fatty Acid Synthase Inhibition in the Ventromedial Nucleus of the Hypothalamus and Accumulation of Malonyl-CoA.” Diabetes 55 (2006): 1327-1336
- Puglisi F, Aprile G, Sobrero A “Tamoxifen-induced total alopecia.” Ann Intern Med 134 (2001): 1154-592.
- Hampson JP, Donnelly A, Lewisjones MS, Pye JK “Tamoxifen-induced hair colour change.” Br J Dermatol 132 (1995): 483-4
- Palmer JL, Trotter T, Joy AA, Carlson LE “Cognitive effects of Tamoxifen in pre-menopausal women with breast cancer compared to healthy controls.” J Cancer Surviv 2 (2008): 275-82
- Forouzanfar MH, Foreman KJ, Delossantos AM, Lozano R, Lopez AD, Murray CJ, Naghavi M. Breast and cervical cancer in 187 countries between 1980 and 2010: a systematic analysis. Lancet 2011; 378: 1461-84.
- Kiyotani K, Mushiroda T, Nakamura Y, Zembutsu H. Pharmacogenomics of tamoxifen: roles of drug metabolizing enzymes and transporters. Drug Metabolism and Pharmacokinetics 2012; 27: 122-31.
- Barakat RR. Tamoxifen and endometrial neoplasia. Clinical Obstetrics and Gynecology 1996; 39:629-640.
- Garuti G. Cellani F, Centinaio G, Sita G, Nalli G, Luerti M. Baseline endometrial assessment before tamoxifen for breast cancer in asymptomatic menopausal women. Gynecologic Oncology 2005; 98: 63 – 67.
- Giorda G, Crivellari D, Veronesi A, Perin T, Campagnutta E, Carbone A, Scarabelli C. Comparison of ultrasonography, hysteroscopy,and biopsy in the diagnosis of endometrial lesions in postmenopausal tamoxifen-treated patients. Acta Obstetricia et Gynecologica Scandinavica 2002:81: 975–980.
- Beşe T, Kösebay D, Demirkiran F, Arvas M, Beşe N, Mandel N. Ultrasonographic appearance of endometrium in postmenopausal breast cancer patients receiving tamoxifen. European Journal of Obstetrics & Gynecology and Reproductive Biology 1996; 67: 157-162.
- Cecchini S, Ciatto S, Bonardi R, Mazzotta A, Grazzini G, Pacini P, Muraca MG. Screening byultrasonography for endometrial carcinoma in postmenopausal breast cancer patients under adjuvant tamoxifen. Gynecological Oncology 1996; 60: 409-411.
- Bingol B, Gunenc MZ, Gedikbasi A, Guner H, Tasdemir S, Tiras B. Comparison of diagnostic accuracy of saline infusion sonohysterography, transvaginal sonography and hysteroscopy in postmenopausal bleeding. Archives of Gynecology and Obstetrics 2011; 284: 111-7.
- Dhaliwal LK, Suri V, Gupta KR, Sahdev: S: Tamoxifen: An alternative to clomiphene in women with polycystic ovary syndrome. Hum Reprod Sci. 2011 May;4(2):76-9.
- Onitilo A, Engel J, Berg R.: epidemiology of tamoxifen and thromboembolism. Clin Med Res. 2011 Nov;9(3-4):150.