INDICE:
Fattori di rischio: sono la precocità di inizio dell’attività sessuale associato ad un elevato numero di partners, le terapie immunosoppressive, sistema immunitario depresso, il basso livello socio-economico (il 70% dei casi di cervicocarcinoma si sviluppa nelle nazioni in via di sviluppo), la multiparità, terapia contraccettiva ormonale, il fumo.
Le infezioni da Papillomavirus (HPV) in particolar modo di  alcuni tipi come il 16 ed il 18 (75%) e, più recentemente, il 31, 33 e 35 (15%) sono coinvolte complessivamente nel 90% dei casi di cervicocarcinoma. Le verruche genitali sono una forma di tumore benigno delle cellule epiteliali e sono causate da vari ceppi di HPV. Tuttavia, questi sierotipi di solito non sono legati al cancro del collo dell’utero. Spesso si ritrovano contemporaneamente lesioni pre-cancerose e verruche.
alcuni tipi come il 16 ed il 18 (75%) e, più recentemente, il 31, 33 e 35 (15%) sono coinvolte complessivamente nel 90% dei casi di cervicocarcinoma. Le verruche genitali sono una forma di tumore benigno delle cellule epiteliali e sono causate da vari ceppi di HPV. Tuttavia, questi sierotipi di solito non sono legati al cancro del collo dell’utero. Spesso si ritrovano contemporaneamente lesioni pre-cancerose e verruche.
Il fumo di sigaretta, sia attivo che passivo, aumenta il rischio di cancro della cervice uterina. Le donne HPV-infettate, attuali e/o ex-fumatrici hanno 2-3 volte maggiore incidenza di cancro invasivo rispetto a un gruppo controllo di non fumatrici. Il fumo passivo è anch’esso associato a un aumentato rischio, ma in percentuali minori [29].
Il fumo può aumentare il rischio di cervicocarcinoma in modo diretto: la fumatrice ha una maggiore probabilità di sviluppare un CIN3 che ha la potenzialità di formare il cancro cervicale. Forti fumatrici a lungo termine sembrano avere un rischio di lesioni CIN3 molto più elevato rispetto al gruppo controllo non fumatrici. Indirettamente il fumo contribuisce ad accrescere il rischio in pazienti HPV positive.
I contraccettivi orali fanno aumentare di cinque volte il rischio di ca cervicale se usati per >5 anni senza soluzione di continuità; il rischio aumenta di 10 volte se i CO sono stati utilizzati in modo continuo per >10 anni.
Gravidanze a termine: le donne che hanno avuto >6 gravidanze a termine, presentano un rischio di ca. cervicale aumentato di 4 volte rispetto ale donne con 1-2 gravidanze a termine.
Diagnosi
Il cervicocarcinoma allo stadio iniziale è spesso asintomatico.
- I sintomi, quando presenti, sono aspecifici: spotting spontaneo o dopo rapporti sessuali, leucorrea maleodorante.
- Il sospetto diagnostico di cervicocarcinoma si pone sulla base di un referto dubbio o positivo all’esame citologico cervicale.
- La colposcopia rappresenta, successivamente, l’esame di secondo livello. Essa utilizza l’acido acetico per valutare la cervice uterina con citologia dubbia o francamente anormale dove eseguire la biopsia per l’esame istologico.

- Dove non sono operativi programmi di screening può accadere che il sospetto di neoplasia cervicale venga posto dopo un esame clinico (forma esofitica con tessuto friabile facilmente sanguinante, forma endofitica con cervice dura; a volte l’esocervice può sembrare integra ed il collo uterino può assumere forma a “barilotto”. Altre volte si può avere la forma ulcerativa, con formazione di un “cratere” più o meno profondo).
- La biopsia cervicale deve essere effettuata su tutte le lesioni clinicamente sospette preferibilmente sotto guida colposcopica. Quando la citologia suggerisce la presenza di una neoplasia cervicale ma non vi è alcuna lesione visibile macroscopicamente o colposcopicamente deve essere effettuata una conizzazione con curettage frazionato. La conizzazione può essere eseguita con: lama fredda, con laser CO2 o con ansa diatermica ad onde radio ad alta frequenza.
La conizzazione cervicale è indicata nelle seguenti condizioni:
- non vi è lesione visibile colposcopicamente
- l’epitelio atipico si estende lungo il canale cervicale e la lesione non può essere adeguatamente visualizzata all’esame colposcopico in tutta la sua estensione
- vi è discrepanza tra il risultato della biopsia eseguita in corso di colposcopia e l’esame citologico
- la diagnosi di microinvasione deriva da una biopsia a morso cervicale
- il curettage endocervicale identifica una CIN.
——————————————————————————————–
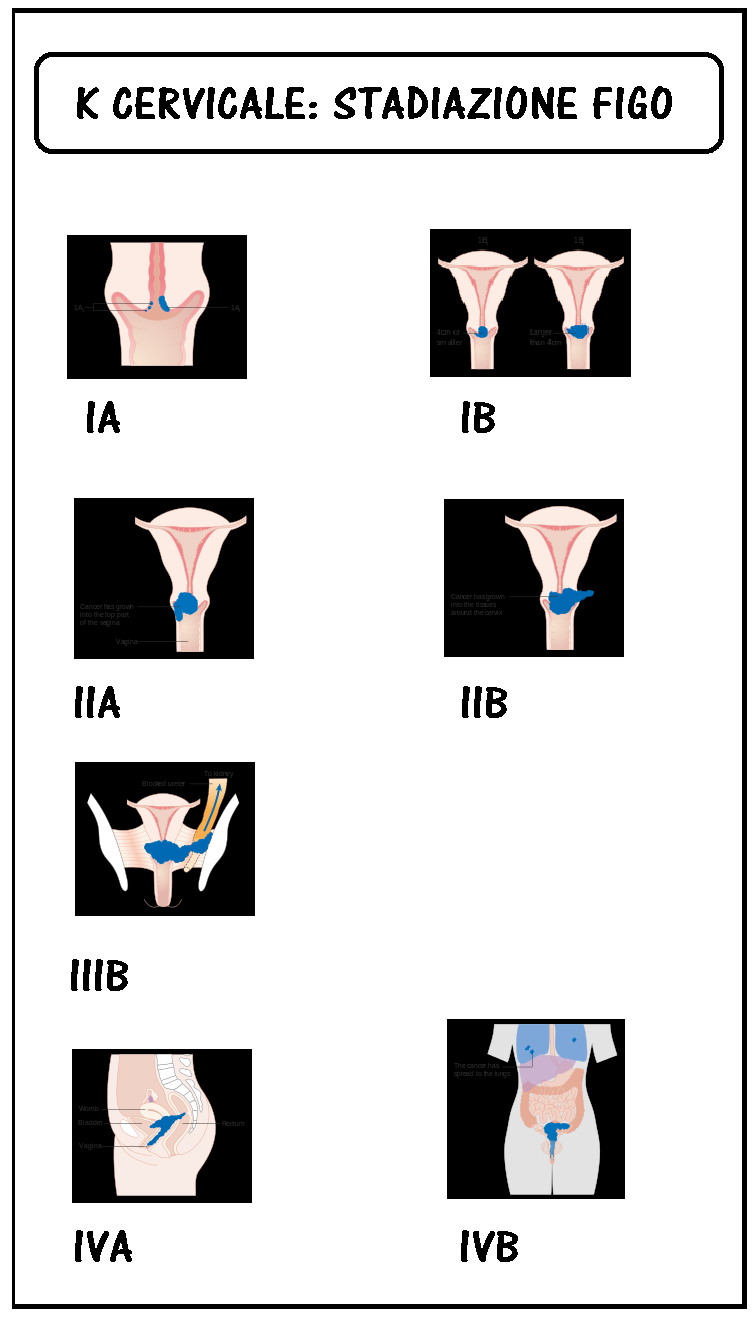
Stadiazione
L’attuale stadiazione del cervicocarcinoma invasivo è quella proposta dalla FIGO a Montreal nel 1994 (vedi tab. 1).
| Stadio O (TO) | Carcinoma in situ, carcicoma intraepiteliale. | ||||||||||||||
|
|||||||||||||||
|
|||||||||||||||
|
|||||||||||||||
|
|||||||||||||||
Le procedure diagnostiche suggerite dalla FIGO per la stadiazione del cervicocarcinoma sono: esame vaginale bimanuale e vagino-rettale (eventualmente in narcosi), colposcopia, biopsia (già citate nelle procedure diagnostiche), Rx torace, urografia. Cistoscopia e proctosigmoidoscopia solo per sospetto clinico di invasione.
Le regole per una corretta stadiazione clinica, secondo la FIGO sono:
– lo stadio deve essere definito clinicamente prima di qualsiasi programma terapeutico
– la stadiazione clinica va effettuata immediatamente dopo la diagnosi di cervicocarcinoma
– definito lo stadio esso non deve essere modificato successivamente
– nei casi di dubbio clinico tra due stadi deve essere scelto lo stadio inferiore.
La stadiazione FIGO basata su dati clinici e strumentali presenta una discrepanza con i dati patologici nel 20-60% dei casi. Lo stadio FIGO non considera il coinvolgimento linfonodale in contrasto con la classificazione TNM.
L’ultrasonografia, la TAC e la RMN proposte per superare i limiti della stadiazione clinica non hanno dimostrato un reale vantaggio.
————————————————————————————–
Classificazione istologica:
- carcinoma a cellule squamose (80-85%)
- adenocarcinoma (circa il 15%)
- carcinoma adenosquamoso
- carcinoma a piccole cellule
- tumore neuroendocrino
- carcinoma a cellule vetrose
- adenocarcinoma villoghiandolare
————————————————————————————————
Fattori prognostici
Utili per un corretto inquadramento nosologico ma non determinanti per la stadiazione. Essi sono:
Stadio: rappresenta uno dei più importanti fattori prognostici; ad esso sono direttamente correlati il rischio di metastasi linfonodali e la sopravvivenza. Sopravvivenza in base allo stadio: Stadio I 85%, Stadio II 66%, Stadio III 39%, Stadio IV 11%.
Profondità di invasione stromale: carattere differenziale tra stadio IA1 (< 3 mm) e stadio IA2 (> 3 < 5 mm). È correlata con il rischio di metastasi linfonodali e di recidiva locale (< 3 mm: N+0,2%; tra 3 e 5 mm: N+6,8%; tra 6 e 10 mm: N+14%; &Mac179; 20 mm: N+46%).
Estensione orizzontale: è correlata dal rischio di metastasi linfonodali e di recidiva locale.
Dimensione del tumore: il diametro cervicale è carattere differenziale tra lo stadio IB1 (&Mac178; 4 cm) e IB2 (&Mac179; 4 cm). È un importante fattore prognostico per l’insorgenza di recidive pelviche e per il rischio di metastasi linfonodali. Alle dimensioni del tumore è correlata la sopravvivenza.
Stato linfonodale: è il principale fattore prognostico a cui sono strettamente correlati sia gli indici di sopravvivenza che le recidive. A parità di stadio, infatti, in presenza di coinvolgimento linfonodale la sopravvivenza è peggiore. La sopravvivenza a 5 anni è dell’85-90% nei casi N- e del 50% in quelli N+.
Diffusione neoplastica negli spazi capillarosimili, ematici e linfatici: sono tutti fattori correlati con il rischio di metastasi linfonodali, con le recidive e con la sopravvivenza.
Tipo istologico, grado di differenziazione, recettori ormonali, virus e oncogeni, modalità di infiltrazione e reazione flogistica peritumorale: oggetto ancora oggi di studio. I risultati sono contraddittori. Non sembrano influire sulla prognosi.
———————————————————————————————-
Terapia
I trattamenti impiegati per il cervicocarcinoma sono principalmente due: la chirurgia e la radioterapia. Queste due modalità di trattamento sono riconosciute come ugualmente efficaci sia per il controllo locale della malattia, sia per i risultati positivi sulla sopravvivenza.
Il trattamento chirurgico è utilizzato prevalentemente quando la malattia è in fase iniziale. Con il progredire dello stadio la terapia prevalentemente utilizzata è quella radiante esterna e brachiterapia. Questa scelta è condizionata anche dall’età della paziente, trattandosi spesso di donne giovani, nelle quali il trattamento radioterapico può influire negativamente sulla funzione endocrina ovarica e sessuale. Il trattamento chirurgico evita le complicazioni legate alle alte dosi radioterapiche ed assume, inoltre, un importante ruolo nella valutazione dei vari fattori istopatologici che hanno un significato prognostico. Recentemente è dedicata particolare attenzione alle donne in età fertile e con K agli stadi iniziali. In questi casi si cerca di risparmiare la funzionalità riproduttiva (“fertility-sparing therapy”) pur rispettando rigorosamente i limiti imposti dalla malattia.
Stadio IA: la FIGO lo suddivide in IA1, comprendente quelle lesioni con invasione stromale inferiore a 3 mm ed estensione orizzontale inferiore a 7 mm e IA2 in cui le lesioni con invasione stromale tra 3 e 5 mm ed estensione orizzontale inferiore a 7 mm. Lo stadio IA può essere trattato con isterectomia ed escissione del colletto vaginale (2 cm). per lo stadio IA2 si aggiunge anche la linfadenectomia pelvica. Per lo stadio IA1 si può anche effettuare la sola conizzazione cervicale (108) oppure una trachelectomia semplice o radicale che include anche l’asportazione di alcuni linfonodi pelvici (104-107).
La diagnosi di carcinoma allo stadio IA non può essere posta sulla base di una semplice biopsia ma è necessario effettuare una conizzazione allo scopo di evidenziare i caratteri essenziali per un corretto inquadramento nosologico. Solo in tal modo è possibile stabilire la profondità di invasione e valutare i fattori prognostici. Per lesioni con invasione <3 mm in assenza di fattori prognostici sfavorevoli una chirurgia conservativa è appropriata, dal momento che il rischio di metastasi linfonodali è estremamente basso (0,2%).
I fattori che possono influire sulla decisione di adottare un trattamento conservativo sono: l’età della paziente, il desiderio di prole, l’assenza di patologia genitale concomitante, la disponibilità ad un adeguato follow-up. Nei casi IA1 con fattori prognostici sfavorevoli il trattamento deve essere personalizzato potendosi effettuare in alternativa un intervento di isterectomia extrafasciale (Piver I).
Nello stadio IA2 il rischio di metastasi linfonodali è del 6,8% e rappresenta il nodo cruciale nella scelta della terapia che non può che essere personalizzata: il trattamento può essere conservativo (conizzazione) o radicale (isterectomia sec. Piver II con linfadenectomia pelvica) oppure con radioterapia pelvica o brachiterapia. In assenza di fattori prognostici sfavorevoli ed in casi selezionati, al fine di conservare la fertilità, può essere consentita l’esecuzione di un’ampia conizzazione purché i margini di resezione chirurgica siano indenni da neoplasia e la paziente offra garanzie di follow-up adeguato.
Il trattamento conservativo determina un rischio di recidiva del’11-12% (sovrapponibile a quello ottenuto con una isterectomia extrafasciale sec. Piver I) e di mortalità del 2-6%.
Il trattamento radicale determina un rischio di recidiva del 2% ed un azzeramento della mortalità. La conizzazione come trattamento definitivo degli stadi IA2 richiede, quindi, alcuni criteri quali:
1) desiderio di mantenimento della fertilità
2) collaborazione della paziente per un adeguato follow-up
3) margini del cono liberi da neoplasia
4) assenza di interessamento degli spazi linfovascolari
5) procedura istopatologica conforme agli standard.
La terapia chirurgica delle lesioni neoplastiche iniziali della portio deve essere personalizzata attuando demolizioni minime con massima garanzia di efficacia.
Stadio IB-IIA: l’isterectomia radicale con linfoadenectomia pelvica sistematica e la radioterapia transcutanea con brachiterapia conseguono gli stessi risultati in termini di sopravvivenza (80-90%).
L’opzione terapeutica è influenzata dall’età, dalla conservazione della funzione ovarica, dalle condizioni generali della paziente.
Le complicanze, anche se qualitativamente differenti, sono sovrapponibili nelle due diverse modalità terapeutiche.
Nelle pazienti irradiate in prima istanza per neoplasia allo stadio IB2 non sarebbe giustificata una isterectomia postradioterapia per l’aumento dei costi e della mortalità senza un evidente vantaggio in termini di controllo locale della malattia.
La chemioterapia neoadiuvante alla radioterapia consente di ottenere risposte obiettive nel 50% dei casi ma non modifica la prognosi né i termini di sopravvivenza né nel controllo locale della malattia. Al contrario incoraggianti sembrano essere i risultati della chemioradioterapia concomitanti.
L’integrazione di chirurgia e radioterapia non ha prodotto alcun incremento terapeutico ma a fronte di una drastica riduzione delle recidive pelviche si assiste ad un significativo incremento delle recidive a distanza senza alcun impatto sulla sopravvivenza.
Stadio IIB: il trattamento standard è la radioterapia esterna con brachiterapia. Tale metodo determina una sopravvivenza a 5 anni tra il 38 ed il 60%. Circa il 30% delle donne allo stadio IIB hanno metastasi ai linfonodi paraaortici.
Alcuni centri trattano tali pazienti con l’isterectomia radicale sec. Piver III con linfoadenectomia pelvica con sopravvivenza assimilabile a quella ottenuta mediante radioterapia.
La linfoadenectomia aortica sembra indicata nei tumori con diametro superiore a 4 cm e con linfonodi pelvici positivi.
Stadio III e IV: la radioterapia esterna e la brachiterapia rappresentano lo standard terapeutico in questi stadi. La sopravvivenza a 5 anni al III stadio è compresa tra il 20 ed il 40%, mentre al IV stadio oscilla tra il 5 ed il 20%.
Cervicocarcinoma invasivo dopo isterectomia semplice: in presenza di cervicocarcinoma invasivo inaspettato dopo isterectomia semplice, effettuata per patologia benigna, in caso di coinvolgimento neoplastico dei margini di resezione deve essere eseguita una radioterapia postoperatoria nel più breve lasso di tempo possibile. Infatti la sopravvivenza di tali pazienti è direttamente correlata alla tempestività del trattamento. Non si deve eseguire un intervento di isterectomia senza avere effettuato un esame colpocitologico.
Carcinoma del moncone: tale neoplasia deve essere trattata come quella insorta su un utero intatto. I risultati sia in termini di cura che di sopravvivenza sono sovrapponibili nei due gruppi di pazienti.
Terapia delle recidive: la terapia di una recidiva varia in base alla terapia precedentemente eseguita ed alla sede della recidiva.
È possibile effettuare una terapia curativa solo nelle pazienti con recidiva pelvica centrale senza segni di metastasi linfonodale o a distanza.
Nelle pazienti trattate con radioterapia in prima istanza è improponibile un secondo trattamento radioterapico per la costante associazione con complicanze inaccettabili. La pelvectomia anteriore, posteriore o totale rappresenta la procedura di scelta nella recidiva pelvica centrale dopo radioterapia primaria in assenza di diffusione extrapelvica del tumore e/o di metastasi linfonodali. Questo intervento, altamente mutilante, comporta una notevole percentuale di complicanze postoperatorie e seri problemi psicologici. Per tali ragioni non deve essere effettuato a scopo palliativo.
Il trattamento delle pazienti con recidiva pelvica centrale dopo intervento chirurgico primario è la radioterapia esterna con RT intracavitaria; in casi selezionati si può ricorrere alla evisceratio pelvica. In caso di recidiva laterale o periferica (invasione dei parametri, fissazione alla parete pelvica, metastasi linfonodali) è indicata la chemioterapia.
FOLLOW-UP
Il follow-up delle pazienti permette di individuare precocemente la comparsa delle recidive, e delle complicanze tardive.
La prognosi di tali pazienti è, infatti, anche legata alla precocità con la quale viene diagnosticata una recidiva. I controlli periferici comprendono l’esame clinico generale e la visita ginecologica vagino-rettale, il Pap-test, gli esami di laboratorio di routine.
Altri esami vanno eseguiti quando richiesti dalla situazione clinica.
È consigliabile una scadenza di quattro mesi per i primi due anni dall’intervento, e di sei mesi fino al quinto anno.
PREVENZIONE:
- Vaccinazione: due i vaccini attualmente commercializzati in Italia: Gardasil e Cervarix. Il vaccino riduce del 90% il rischio di K cervicale.
- Rapporti sessuali protetti
- Dieta: l’assunzione di Vitamina A è associata con basso rischio di K cervicale come pure la vitamina B12, vitamina C, vitamina E, beta-carotene (109-110).
References:
- “Defining Cancer”. National Cancer Institute. Retrieved 10 June 2014.
- Tarney, CM; Han, J (2014). “Postcoital bleeding: a review on etiology, diagnosis, and management.”. Obstetrics and Gynecology International. 2014: 192087. doi:10.1155/2014/192087. PMID 25045355.
- Kumar V, Abbas AK, Fausto N, Mitchell RN (2007). Robbins Basic Pathology (8th ed.). Saunders Elsevier. pp. 718–721. ISBN 978-1-4160-2973-1.
- Kufe, Donald (2009). Holland-Frei cancer medicine. (8th ed.). New York: McGraw-Hill Medical. p. 1299. ISBN 9781607950141.
- World Cancer Report 2014. World Health Organization. 2014. pp. Chapter 5.12. ISBN 9283204298.
- Dunne, EF; Park, IU (Dec 2013). “HPV and HPV-associated diseases.”.Infectious Disease Clinics of North America. 27 (4): 765–78.doi:10.1016/j.idc.2013.09.001. PMID 24275269.
- “Cervical Cancer Treatment (PDQ®)”. National Cancer Institute. 2014-03-14. Retrieved 25 June 2014.
- “FDA approves Gardasil 9 for prevention of certain cancers caused by five additional types of HPV”. U.S. Food and Drug Administration. 10 December 2014. Retrieved 8 March 2015.
- “Human Papillomavirus (HPV) Vaccines”. National Cancer Institute. 2011-12-29. Retrieved 25 June 2014.
- Tran, NP; Hung, CF; Roden, R; Wu, TC (2014). “Control of HPV infection and related cancer through vaccination.”. Recent Results in Cancer Research. 193: 149–71. doi:10.1007/978-3-642-38965-8_9. PMID 24008298.
- “Cervical Cancer Prevention (PDQ®)”. National Cancer Institute. 2014-02-27. Retrieved 25 June 2014.
- World Health Organization (February 2014). “Fact sheet No. 297: Cancer”. Retrieved 2014-06-24.
- “SEER Stat Fact Sheets: Cervix Uteri Cancer”. NCI. Retrieved 18 June2014.
- World Cancer Report 2014. World Health Organization. 2014. pp. Chapter 1.1. ISBN 9283204298.
- Canavan TP, Doshi NR (2000). “Cervical cancer”. Am Fam Physician.61 (5): 1369–76. PMID 10735343.
- Jr, Charles E. Carraher (2014). Carraher’s polymer chemistry (Ninth ed.). Boca Raton: Taylor & Francis. p. 385. ISBN 9781466552036.
- Nanda, Rita (2006-06-09). “Cervical cancer”. MedlinePlus Medical Encyclopedia. National Institutes of Health. Retrieved 2007-12-02.
- “Cervical Cancer Prevention and Early Detection”. Cancer.
- Gadducci A, Barsotti C, Cosio S, Domenici L, Riccardo Genazzani A (2011). “Smoking habit, immune suppression, oral contraceptive use, and hormone replacement therapy use and cervical carcinogenesis: A review of the literature”. Gynecological Endocrinology. 27 (8): 597–604.doi:10.3109/09513590.2011.558953. PMID 21438669.
- Stuart Campbell; Ash Monga (2006). Gynaecology by Ten Teachers (18 ed.). Hodder Education. ISBN 0-340-81662-7.
- Dillman, edited by Robert K. Oldham, Robert O. (2009). Principles of cancer biotherapy (5th ed.). Dordrecht: Springer. p. 149. ISBN 9789048122899.
- “What Causes Cancer of the Cervix?”. American Cancer Society. 2006-11-30. Archived from the original on 2007-10-13. Retrieved 2007-12-02.
- Marrazzo JM, Koutsky LA, Kiviat NB, Kuypers JM, Stine K (2001).“Papanicolaou test screening and prevalence of genital human papillomavirus among women who have sex with women”. Am J Public Health. 91 (6): 947–52. doi:10.2105/AJPH.91.6.947. PMC 1446473
 . PMID 11392939.
. PMID 11392939. - “HPV Type-Detect”. Medical Diagnostic Laboratories. 2007-10-30. Archived from the original on 2007-09-27. Retrieved 2007-12-02.
- Gottlieb, Nicole (2002-04-24). “A Primer on HPV”. Benchmarks. National Cancer Institute. Retrieved 2007-12-02.
- Muñoz N, Bosch FX, de Sanjosé S, Herrero R, Castellsagué X, Shah KV, Snijders PJ, Meijer CJ (2003). “Epidemiologic classification of human papillomavirus types associated with cervical cancer”. N. Engl. J. Med. 348 (6): 518–27. doi:10.1056/NEJMoa021641. PMID 12571259.
- Snijders PJ, Steenbergen RD, Heideman DA, Meijer CJ (2006). “HPV-mediated cervical carcinogenesis: concepts and clinical implications”. J. Pathol.208 (2): 152–64. doi:10.1002/path.1866. PMID 16362994.
- National Institutes of Health, National Cancer Institute: PDQ®Cervical Cancer Prevention. Bethesda, MD: National Cancer Institute. Date last modified 12/17/2015. Accessed 05/20/2015.
- Luhn P, Walker J, Schiffman M, Zuna RE, Dunn ST, Gold MA, Smith K, Mathews C, Allen RA, Zhang R, Wang S, Wentzensen N (2013). “The role of co-factors in the progression from human papillomavirus infection to cervical cancer”. Gynecologic Oncology. 128 (2): 265–270.doi:10.1016/j.ygyno.2012.11.003. ISSN 0090-8258. PMID 23146688.
- Remschmidt C, Kaufmann AM, Hagemann I, Vartazarova E, Wichmann O, Deleré Y (2013). “Risk Factors for Cervical Human Papillomavirus Infection and High-Grade Intraepithelial Lesion in Women Aged 20 to 31 Years in Germany”.International Journal of Gynecological Cancer. 23 (3): 519–526.doi:10.1097/IGC.0b013e318285a4b2. ISSN 1048-891X. PMID 23360813.
- Gadducci A, Barsotti C, Cosio S, Domenici L, Riccardo Genazzani A (2011). “Smoking habit, immune suppression, oral contraceptive use, and hormone replacement therapy use and cervical carcinogenesis: a review of the literature”. Gynecological Endocrinology. 27 (8): 597–604.doi:10.3109/09513590.2011.558953. ISSN 0951-3590. PMID 21438669.
- Agorastos T, Miliaras D, Lambropoulos AF, Chrisafi S, Kotsis A, Manthos A, Bontis J (2005). “Detection and typing of human papillomavirus DNA in uterine cervices with coexistent grade I and grade III intraepithelial neoplasia: biologic progression or independent lesions?”. European Journal of Obstetrics & Gynecology and Reproductive Biology. 121 (1): 99–103.doi:10.1016/j.ejogrb.2004.11.024. ISSN 0301-2115. PMID 15949888.
- Jensen KE, Schmiedel S, Frederiksen K, Norrild B, Iftner T, Kjær SK (2012). “Risk for cervical intraepithelial neoplasia grade 3 or worse in relation to smoking among women with persistent human papillomavirus infection”.Cancer Epidemiology, Biomarkers & Prevention. 21 (11): 1949–55.doi:10.1158/1055-9965.EPI-12-0663. PMC 3970163
 . PMID 23019238.
. PMID 23019238. - Cecil Medicine: Expert Consult Premium Edition . ISBN 1437736084, 9781437736083. Page 1317.
- Berek and Hacker’s Gynecologic Oncology. ISBN 0781795125, 9780781795128. Page 342
- H. K. Pannu; F. M. Corl; E. K. Fishman (September–October 2001). “CT evaluation of cervical cancer: spectrum of disease”. Radiographics. 21 (5): 1155–1168. doi:10.1148/radiographics.21.5.g01se311155. PMID 11553823.
- “Cancer Research UK website”. Retrieved 2009-01-03.
- DeMay, M (2007). Practical principles of cytopathology. Revised edition. Chicago, IL: American Society for Clinical Pathology Press. ISBN 978-0-89189-549-7.
- Garcia A, Hamid O, El-Khoueiry A (2006-07-06). “Cervical Cancer”.eMedicine. WebMD. Retrieved 2007-12-02.
- Dolinsky, Christopher (2006-07-17). “Cervical Cancer: The Basics”.OncoLink. Abramson Cancer Center of the University of Pennsylvania. Retrieved2007-12-02.
- Arbyn M, Anttila A, Jordan J, Ronco G, Schenck U, Segnan N, Wiener H, Herbert A, von Karsa L (2010). “European Guidelines for Quality Assurance in Cervical Cancer Screening. Second Edition—Summary Document”. Annals of Oncology. 21 (3): 448–458. doi:10.1093/annonc/mdp471. PMC 2826099
 .PMID 20176693.
.PMID 20176693. - Everett T, Bryant A, Griffin MF, Martin-Hirsch PP, Forbes CA, Jepson RG (2011). Everett T, ed. “Interventions targeted at women to encourage the uptake of cervical screening”. Cochrane Database Syst Rev (5): CD002834.doi:10.1002/14651858.CD002834.pub2. PMID 21563135.
- Arbyn M, Anttila A, Jordan J, Ronco G, Schenck U, Segnan N, Wiener H, Herbert A, von Karsa L (Mar 2010). “European Guidelines for Quality Assurance in Cervical Cancer Screening. Second edition–summary document.”. Annals of Oncology. 21 (3): 448–58. doi:10.1093/annonc/mdp471. PMC 2826099.
- “Cervical Cancer Screening Guidelines for Average-Risk Women”(PDF). cdc.gov. Retrieved 8 November 2014.
- “ACOG Practice Bulletin Number 131: Screening for cervical cancer.”.Obstetrics and Gynecology. 120 (5): 1222–38. Nov 2012.doi:10.1097/AOG.0b013e318277c92a. PMID 23090560.
- Karjane N, Chelmow D (June 2013). “New cervical cancer screening guidelines, again”. Obstetrics and Gynecology Clinics of North America. 40 (2): 211–23. doi:10.1016/j.ogc.2013.03.001. PMID 23732026.
- Payne N, Chilcott J, McGoogan E (2000). “Liquid-based cytology in cervical screening: a rapid and systematic review”. Health Technology Assessment. 4(18): 1–73. PMID 10932023.
- Karnon J, Peters J, Platt J, Chilcott J, McGoogan E, Brewer N (May 2004). “Liquid-based cytology in cervical screening: an updated rapid and systematic review and economic analysis”. Health Technology Assessment. 8 (20): iii, 1–78. doi:10.3310/hta8200. PMID 15147611.
- “Liquid Based Cytology (LBC): NHS Cervical Screening Programme”. Retrieved 2010-10-01.
- Moyer VA (Jun 19, 2012). “Screening for cervical cancer: u.s. Preventive services task force recommendation statement”. Annals of Internal Medicine.156 (12): 880–91. doi:10.7326/0003-4819-156-12-201206190-00424.PMID 22711081.
- World Health Organization (2014). Comprehensive cervical cancer control. A guide to essential practice – Second edition. ISBN 978-92-4-154895-3.
- Manhart LE, Koutsky LA (2002). “Do condoms prevent genital HPV infection, external genital warts, or cervical neoplasia? A meta-analysis”. Sex Transm Dis. 29 (11): 725–35. doi:10.1097/00007435-200211000-00018.PMID 12438912.
- Hogewoning CJ, Bleeker MC, van den Brule AJ, Voorhorst FJ, Snijders PJ, Berkhof J, Westenend PJ, Meijer CJ (2003). “Condom use Promotes the Regression of Cervical Intraepithelial Neoplasia and Clearance of HPV: Randomized Clinical Trial”. International Journal of Cancer. 107 (5): 811–816.doi:10.1002/ijc.11474. PMID 14566832.
- “Semen can worsen cervical cancer”. Medical Research Council (UK). Retrieved 2007-12-02.
- Medeiros LR, Rosa DD, da Rosa MI, Bozzetti MC, Zanini RR (2009). “Efficacy of Human Papillomavirus Vaccines”. International Journal of Gynecological Cancer. 19 (7): 1166–76. doi:10.1111/IGC.0b013e3181a3d100.PMID 19823051.
- “Human Papillomavirus (HPV) Vaccines: Q & A”. Fact Sheets: Risk Factors and Possible Causes. National Cancer Institute (NCI). 2009-10-22. Retrieved 2009-11-11.
- Harper D, Gall S, Naud P, Quint W, Dubin G, Jenkins D, et al. (2008). “Sustained immunogenicity and high efficacy against HPV 16/18 related cervical neoplasia: Long-term follow up through 6.4 years in women vaccinated with Cervarix (GSK’s HPV-16/18 AS04 candidate vaccine)”. Gynecol Oncol. 109: 158–159. doi:10.1016/j.ygyno.2008.02.017.
- “Committee opinion no. 467: human papillomavirus vaccination”. Obstet Gynecol. 116 (3): 800–3. Sep 2010. doi:10.1097/AOG.0b013e3181f680c8.PMID 20733476.
- The Asahi Shimbun (15 June 2013). “Health ministry withdraws recommendation for cervical cancer vaccine”. The Asahi Shimbun.
- Zhang X, Dai B, Zhang B, Wang Z (2011). “Vitamin A and risk of cervical cancer: A meta-analysis”. Gynecologic Oncology. 124 (2): 366–73.doi:10.1016/j.ygyno.2011.10.012. PMID 22005522.
- Myung SK, Ju W, Kim SC, Kim H (2011). “Vitamin or antioxidant intake (or serum level) and risk of cervical neoplasm: A meta-analysis”. BJOG. 118 (11): 1285–91. doi:10.1111/j.1471-0528.2011.03032.x. PMID 21749626.
- Erstad, Shannon (2007-01-12). “Cone biopsy (conization) for abnormal cervical cell changes”. WebMD. Retrieved 2007-12-02.
- Jones WB, Mercer GO, Lewis JL, Rubin SC, Hoskins WJ (1993). “Early invasive carcinoma of the cervix”. Gynecol. Oncol. 51 (1): 26–32.doi:10.1006/gyno.1993.1241. PMID 8244170.
- Dolson, Laura (2001). “Trachelectomy”. Retrieved 2007-12-02.
- Burnett AF (2006). “Radical trachelectomy with laparoscopic lymphadenectomy: review of oncologic and obstetrical outcomes”. Curr. Opin. Obstet. Gynecol. 18 (1): 8–13. doi:10.1097/01.gco.0000192968.75190.dc.PMID 16493253.
- Cibula D, Ungár L, Svárovský J, Zivný J, Freitag P (2005). “[Abdominal radical trachelectomy–technique and experience]”. Ceska Gynekol (in Czech). 70 (2): 117–22. PMID 15918265.
- Plante M, Renaud MC, Hoskins IA, Roy M (2005). “Vaginal radical trachelectomy: a valuable fertility-preserving option in the management of early-stage cervical cancer. A series of 50 pregnancies and review of the literature”.Gynecol. Oncol. 98 (1): 3–10. doi:10.1016/j.ygyno.2005.04.014.PMID 15936061.
- Roy M, Plante M, Renaud MC, Têtu B (1996). “Vaginal radical hysterectomy versus abdominal radical hysterectomy in the treatment of early-stage cervical cancer”. Gynecol. Oncol. 62 (3): 336–9. doi:10.1006/gyno.1996.0245.PMID 8812529.
- Dargent D, Martin X, Sacchetoni A, Mathevet P (2000). “Laparoscopic vaginal radical trachelectomy: a treatment to preserve the fertility of cervical carcinoma patients”. Cancer. 88 (8): 1877–82. doi:10.1002/(SICI)1097-0142(20000415)88:8<1877::AID-CNCR17>3.0.CO;2-W. PMID 10760765.
- Schlaerth JB, Spirtos NM, Schlaerth AC (2003). “Radical trachelectomy and pelvic lymphadenectomy with uterine preservation in the treatment of cervical cancer”. Am. J. Obstet. Gynecol. 188 (1): 29–34. doi:10.1067/mob.2003.124.PMID 12548192.
- Waggoner, Steven E (2003). “Cervical Cancer”. The Lancet. 361 (9376): 2217–25. doi:10.1016/S0140-6736(03)13778-6.
- “FDA Approves First Drug Treatment for Late-Stage Cervical Cancer”. U.S. Food and Drug Administration. 2006-06-15. Retrieved 2007-12-02.
- Sardain, H; Lavoue, V; Redpath, M; Bertheuil, N; Foucher, F; Levêque, J (August 2015). “Curative pelvic exenteration for recurrent cervical carcinoma in the era of concurrent chemotherapy and radiation therapy. A systematic review.”. European journal of surgical oncology : the journal of the European Society of Surgical Oncology and the British Association of Surgical Oncology.41 (8): 975–85. doi:10.1016/j.ejso.2015.03.235. PMID 25922209.
- “Cervical Cancer”. Encyclopedia of Women’s Health.
- “What Are the Key Statistics About Cervical Cancer?”. American Cancer Society. 2006-08-04. Archived from the original on 2007-10-30. Retrieved2007-12-02.
- “Cervical Cancer”. Cervical Cancer: Cancers of the Female Reproductive System: Merck Manual Home Edition. Merck Manual Home Edition. Retrieved2007-03-24.
- Committee on Practice Bulletins-Gynecology (2002). “ACOG practice bulletin. Diagnosis and treatment of cervical carcinomas, number 35, May 2002”.Obstetrics and gynecology. 99 (5 Pt 1): 855–67. PMID 11978302.
- “Cervical Cancer”. Cervical Cancer: Pathology, Symptoms and Signs, Diagnosis, Prognosis and Treatment. Armenian Health Network, Health.am.
- (SEER Cancer Statistics Review 1975-2000, National Cancer Institute (NCI)).
- “Cervical cancer statistics and prognosis”. Cancer Research UK. Retrieved2007-03-24.
- Nygård M (2011). “Screening for cervical cancer: When theory meets reality”. BMC Cancer. 11: 240. doi:10.1186/1471-2407-11-240.PMC 3146446
 . PMID 21668947.
. PMID 21668947. - “WHO Disease and injury country estimates”. World Health Organization. 2009. Retrieved Nov 11, 2009.
- Kent A (Winter 2010). “HPV Vaccination and Testing.”. Reviews in Obstetrics and Gynecology. 3 (1): 33–4. PMC 2876324
 . PMID 20508781.
. PMID 20508781. - Howlader (November 10, 2014). “SEER Stat Fact Sheets: Cervix Uteri”.National Cancer Institute. Retrieved 7 February 2012.
- Armstrong EP (April 2010). “Prophylaxis of Cervical Cancer and Related Cervical Disease: A Review of the Cost-Effectiveness of Vaccination Against Oncogenic HPV Types”. Journal of Managed Care Pharmacy. 16 (3): 217–30.PMID 20331326.
- “Cervical cancer statistics”. Cancer Research UK. Retrieved 27 October2014.
- MacDonald N, Stanbrook MB, Hébert PC (September 2008). “Human papillomavirus vaccine risk and reality”. CMAJ (in French). 179 (6): 503-505.
- National Cancer Registry Programme under Indian Council of Medical Research Reports
- Krishnatreya, M; Kataki, AC; Sharma, JD; Nandy, P; Gogoi, G (2015). “Association of educational levels with survival in Indian patients with cancer of the uterine cervix.”. Asian Pacific Journal of Cancer Prevention. 16 (8): 3121–3.doi:10.7314/apjcp.2015.16.8.3121. PMID 25921107.
- zur Hausen, Harald (2002). “Papillomaviruses and cancer: from basic studies to clinical application”. Nature Reviews Cancer. 2 (5): 342–350.doi:10.1038/nrc798. ISSN 1474-1768.
- Menczer, J (February 2003). “The low incidence of cervical cancer in Jewish women: has the puzzle finally been solved?”. The Israel Medical Association journal : IMAJ. 5 (2): 120–3. PMID 12674663. Retrieved 28 November 2015.
- Heins HC, Dennis EJ, Pratthomas HR (1958). “The possible role of smegma in carcinoma of the cervix”. American Journal of Obstetrics & Gynecology. 76(4): 726–33. PMID 13583012.
- Alexander ER (1973). “Possible Etiologies of Cancer of the Cervix Other Than Herpesvirus”. Cancer Research. 33 (6): 1485–90. PMID 4352386.
- Dürst M, Gissmann L, Ikenberg H, zur Hausen H (1983). “A papillomavirus DNA from a cervical carcinoma and its prevalence in cancer biopsy samples from different geographic regions”. Proceedings of the National Academy of Sciences of the United States of America. 80 (12): 3812–5.doi:10.1073/pnas.80.12.3812. PMC 394142
 . PMID 6304740..
. PMID 6304740.. - Lowy DR, Schiller JT (2006). “Prophylactic human papillomavirus vaccines”.J. Clin. Invest. 116 (5): 1167–73. doi:10.1172/JCI28607. PMC 1451224
 .PMID 16670757.
.PMID 16670757. - McNeil C (April 2006). “Who invented the VLP cervical cancer vaccines?”. J. Natl. Cancer Inst. 98 (7): 433. doi:10.1093/jnci/djj144. PMID 16595773.PMID 16595773
- Cancer Institute NSW (2013). “Information about cervical screening for Aboriginal women”. NSW Government. Archived from the original on 11 April 2013.
- Mary-Anne Romano (17 October 2011). “Aboriginal cervical cancer rates parallel health inequity”. Science Network Western Australia. Archived fromthe original on 14 May 2013.
- Australian Cervical Cancer Foundation. “Vision and Mission”. Australian Cervical Cancer Foundation. Archived from the original on 12 May 2013.
- Australian Cervical Cancer Foundation. “Our People”. Australian Cervical Cancer Foundation. Archived from the original on 12 May 2013.
- “Cervical Cancer Treatment (PDQ®)”. NCI. 2014-03-14. Retrieved 24 June 2014.
- Gillian Bradford (16 October 2006). “Janette Howard speaks on her battle with cervical cancer”. Australian Broadcasting Corporation. Archived from the original on 13 November 2012.
- Tiro JA, Meissner HI, Kobrin S, Chollette V (2007). “What do women in the U.S. know about human papillomavirus and cervical cancer?”. Cancer Epidemiol. Biomarkers Prev. 16 (2): 288–94. doi:10.1158/1055-9965.EPI-06-0756. PMID 17267388.
- Dolson, Laura (2001). “Trachelectomy”. Retrieved 2007-12-02.
- Burnett AF (2006). “Radical trachelectomy with laparoscopic lymphadenectomy: review of oncologic and obstetrical outcomes”. Curr. Opin. Obstet. Gynecol. 18 (1): 8–13
- Cibula D, Ungár L, Svárovský J, Zivný J, Freitag P (2005). “[Abdominal radical trachelectomy–technique and experience]”. Ceska Gynekol (in Czech). 70 (2): 117–22. PMID 15918265.
- Jump up^ Plante M, Renaud MC, Hoskins IA, Roy M (2005). “Vaginal radical trachelectomy: a valuable fertility-preserving option in the management of early-stage cervical cancer. A series of 50 pregnancies and review of the literature”.Gynecol. Oncol. 98 (1): 3–10.
- Jump up^ Erstad, Shannon (2007-01-12). “Cone biopsy (conization) for abnormal cervical cell changes”. WebMD. Retrieved 2007-12-02.
- Zhang X, Dai B, Zhang B, Wang Z (2011). “Vitamin A and risk of cervical cancer: A meta-analysis”. Gynecologic Oncology. 124 (2): 366–73.doi:10.1016/j.ygyno.2011.10.012. PMID 22005522.
- Jump up^ Myung SK, Ju W, Kim SC, Kim H (2011). “Vitamin or antioxidant intake (or serum level) and risk of cervical neoplasm: A meta-analysis”. BJOG. 118 (11): 1285–91. doi:10.1111/j.1471-0528.2011.03032.x. PMID 21749626.