Aggiornamento ultimo 22/09/2019 17:10:26
Amenorrea è l’assenza di flussi mestruali. Si definisce amenorrea primaria l’assenza del menarca oltre i 16-18 anni oppure 2 anni dopo lo sviluppo puberale (telarca, pubarca e crescita ossea e staturale). Lo sviluppo puberale avviene all’età di circa 12-13 anni nell’Europa Occidentale.
Per amenorrea secondaria si intende l’assenza di mestruazioni, in pazienti in età fertile, per un periodo ≥90 giorni.
Criptomenorrea invece è il termine utilizzato per definire una mestruazione regolarmente costituita in cui non si verifica la fuoriuscita delle perdite ematiche a causa di ostacoli meccanici come imene imperforato, setti vaginali completi, agenesia vaginale, stenosi o assenza del collo dell’utero, sinechie uterine (1).
Il capitolo delle amenorree è un dedalo complesso e per orientarci utilizziamo tabelle schematiche riassuntive in modo da ottenere una classificazione ed un primo orientamento etiologico. Successivamente saranno trattate le singole patologie.
| Classificazione delle amenorree su base compartimentale | |
| Compartimento I |
utero-vaginale |
| Compartimento II |
ovaio |
| Compartimento III |
ipofisi anteriore |
| Compartimento IV |
SNC |
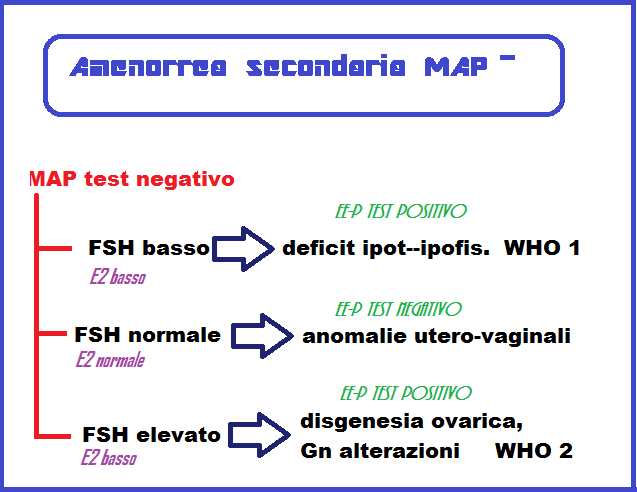
Classificazione dell’amenorrea secondaria in base alla risposta al MAP test
MAP test: si esegue somministrando MAP (Medrossi Progesterone Acetato: Farlutal® cpr 10 mg, 20 mg, 250 mg, 500 mg; sospensione orale 500 mg, 1 gr; fiale im 150 mg, 500 mg, 1 gr) 100 mg intramuscolo o 10 mg/die x 5 giorni per os allo scopo di provocare la mestruazione in caso di amenorrea secondaria.
Se la mestruazione si verifica, in genere entro 10 gg dopo l’ultima somministrazione del farmaco, si possono escludere lesioni delle basse vie genitali. Inoltre è in circolo una sufficiente quantità di estrogeni e quindi e si conferma una funzionalità seppur minima dell’ipotalamo, ipofisi ed ovaio. Ciò vuol dire che la mancanza di progesterone endogeno e quindi di un corpo luteo funzionante è legata all’anovulazione che potrebbe avere diverse cause:
– se la prolattina è normale e c’è assenza di galattorrea significa che la coordinazione ipotalamo-ipofisi-ovario è disturbata da alterazione del sistema feed-back. Si potrà quindi supporre ad es. una policistosi ovarica la cui diagnosi si basa sulle evidenza cliniche, quadro ormonale (LH elevato, FSH normale o basso, FSH/LH alterato in favore di quest’ultimo, estrogeni e androgeni elevati); scansione ecografica e laparoscopia che, oltre a confermare la diagnosi di PCOS possono escludere eventuali tumori funzionali.
– Se c’è invece iperprolattinemia e/o galattorrea, ci troveremo di fronte o ad amenorree iperprolattinemiche o a sindromi amenorrea e galattorrea. In questi casi è d’obbligo la TAC della sella turcica.
– in caso di TSH e Prolattina normali, LH basso o normale, si deve ipotizzare un’insufficienza ipotalamica.
– Distiroidismo in caso di alterazione di TSH, fT3, fT4, Reverse T3 (RT3) presenza di anticorpi anti tireoperossidasi (Ab anti-TPO), Iodiemia, Tireoglobulina (HTG), Ab anti-TBG
In caso di scarse perdite ematiche il risultato del MAP test è da considerarsi dubbio; in caso di mancata mestruazione, occorre ripetere il test dopo 15 giorni.
Il mancato sanguinamento (MAP-test negativo) è indice di:
- ridotta secrezione di estrogeni per disfunzione ipotalamo-ipofisaria, ovarica o tiroidea (vedi schema sovrastante)
- endometrite cronica
- Sindrome di Ascherman
- Alterazioni ostruttive congenite o acquisite utero-cervico-vaginali
Test con estro-progestinici – è utilizzato in caso di MAP test negativo (ovviamente escludendo gravidanza e allattamento). Consiste in somministrazione sequenziale prima di estrogeni (Etinil-estradiolo 20 µg per 25 giorni e poi di progestinici (MAP 10 mg) per 10 giorni. Spesso sono necessari 2 cicli di somministrazione.
La comparsa del flusso mestruale esclude ovviamente una patologia uterina e indirizza alla valutazione della funzionalità ovarica, ipotalamo-ipofisaria e tiroidea.
In caso di mancato flusso mestruale, dopo test EE-P, con FSH ed estradiolo normali, la patologia è da ricercare in anomalie utero-vaginali.
In caso di EE-P negativo con FSH elevato ed estradiolo basso, si devono ipotizzare disgenesia ovarica e/o alterazioni delle gonadotropine (amenorrea WHO 2).
In caso di EE-P test positivo, se FSH ed estradiolo sono inferiori alla norma, si deve ipotizzare una disfunzione ipotalamo-ipofisaria (amenorrea WHO 1, ipogonadismo ipogonadotropo). In questi casi è necessario identificare la causa, funzionale o organica, e la sede (ipotalamica o ipofisaria) della condizione che determina anovulatorietà.
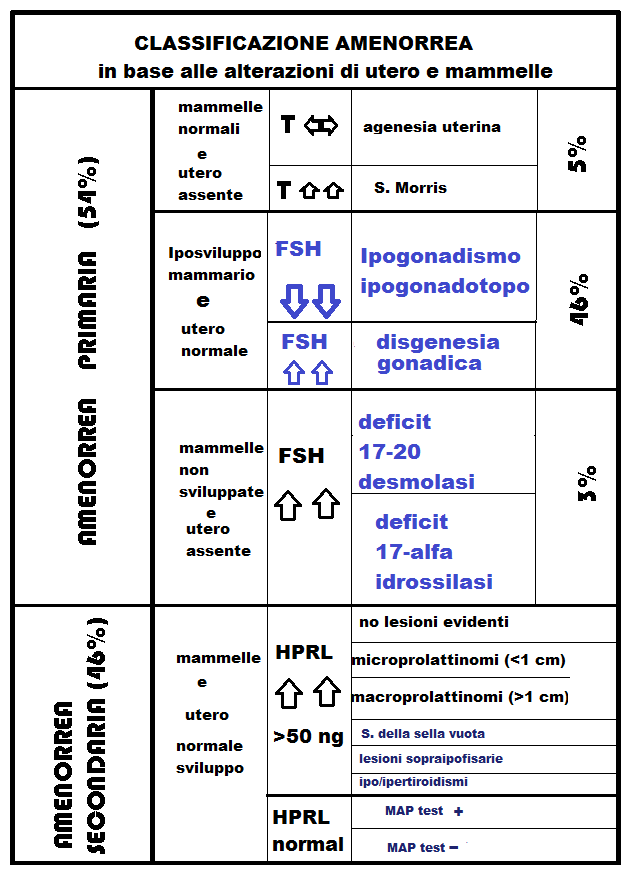
Classificazione amenorrea in base alla presenza di utero e mammelle
 Altra classificazione utile per la diagnosi dell’amenorrea secondaria si avvale del profilo gonadotropinico.
Altra classificazione utile per la diagnosi dell’amenorrea secondaria si avvale del profilo gonadotropinico.
PRESIDI DIAGNOSTICI DI BASE
Anamnesi:
- cronologia dello sviluppo sessuale: adrenarca, telarca e menarca.
- Epoca di insorgenza delle irregolarità mestruali: il verificarsi di cicli mestruali irregolari fin dal menarca suggerisce una diagnosi di PCOS.
- Diete: l’amenorrea in seguito a perdita eccessiva di peso orienta per un’amenorrea da anovulazione ipotalamica in cui il processo etiologico fondamentale è la perdita della secrezione pulsatile di Gn-RH.
Esame obiettivo:
- Esame della vulva, esame della vagina utilizzando uno speculum per vergini e, se possibile, una esplorazione vaginale con un dito.
- Valutare la statura, il peso, il seno, i peli pubici ed ascellari; la bassa statura ci indurrà a sospettare di sindrome di Turner o mosaicismi turneriani.
- palpazione della tiroide
- esame della cute: può evidenziare presenza di strie cutanee, acanthosis nigricans, irsutismo.
- l’altezza, il peso e il BMI ci riveleranno eventuali alterazioni nutritive;
Esami di laboratorio:
- Cariotipo
- Monitoraggio ormonale di base (elevati livelli sierici di Androstenedione e LH ci orienterà per la diagnosi di PCOS)
- FSH, LH, HPRL, E2, E1, T, DHT, DHEA, DHEA-s, C
- MAP test, EE-P test
- USG: per valutare
- la presenza e le dimensioni dell’utero e lo spessore dell’endometrio. In pubertà l’utero ha un DL > 35 mm, il rapporto corpo/collo comincia a delinearsi in favore del primo.
- i diametri ovarici e la riserva follicolare: in condizioni di normalità si evidenziano >7 follicoli secondari al 7° giorno del ciclo
- il rapporto stroma/corticale ovarico
AMENORREA DA PATOLOGIA UTERO-VAGINALE
AMENORREA DA PATOLOGIA OVARICA: comprendono disgenesie gonadiche, senescenza ovarica precoce (POF), patologia ovarica iatrogena, PCOS, neoplasie ovariche
DISGENESIE OVARICHE:
- Sindrome di Turner e Sindromi turneriane (v. file)
- S. della tripla X (47,XXX) (vedi file)
- S. di Morris o femminilizzazione testicolare o S. da deficit recettoriale agli androgeni (45,XY) (v. file)
- Sindrome di Swyer
- S. dell’ipoplasia ovarica congenita o acquisita (46,XX)
- S. dell’ovaio resistente o S. di Savage (46,XX):
La sindrome dell’ovaio resistente (SOR) o sindrome di Savage (dal nome della prima paziente alla quale fu diagnosticata tale patologia) è una sindrome caratterizzata fondamentalmente da oligo/amenorrea ipergonadotropa da insensibilità ovarica alle gonadotropine (27-36).
- Sindrome di Turner (30)
- Sindrome di Swyer (31)
- Sindrome di insensibilità androgena associata a sindrome del cromosoma X fragile (FMR1 gene premutation Xq27.3) (32)
- Mutazioni dei recettori per le gonadotropine FSH ed LH
B) Difetti enzimatici e metabolici ereditari
- Galattosemia: la galattosemia ereditaria (1/20.000 neonati) è una malattia genetica biochimica causata dal deficit dell’enzima galattosio-1-fosfato uridiltransferasi (ALT). Si manifesta in neonati con entrambi i genitori portatori sani della patologia. Manifestazioni acute si verificano nel periodo neonatale, quasi sempre associate all’ingestione del latte: vomito, ittero, cirrosi epatica, diatesi emorragica, anemia, difetto di crescita staturale, nefropatia tubulare, cataratta, encefalopatia, sepsi da E. coli e morte neonatale. Manifestazioni croniche coinvolgono il cervello con conseguente ritardo e disturbi del linguaggio e problemi di apprendimento; l’ovaio risulta danneggiato e iporesponsivo con conseguente ipogonadismo ipergonadotropo. Ci sono alcune segnalazioni di pazienti con corredo follicolare presente, anche se ridotto, e gravidanze a termine. La sorveglianza clinica comprende lo screening per anomalie nella funzione ovarica in età precoce. Il trattamento consiste in supplementazione di estrogeni e progesterone (67-70).
- Talassemia maggiore trattata con trasfusioni multiple
- Emocromatosi, spesso conseguente a trasfusioni continue e prolungate.
C) Altre cause di SOR:
- Infezioni virali in utero
- Secrezione o azione anomala delle gonadotropine
- Patologie autoimmuni (37)
- Disfunzione della tiroide
- Disfunzione polighiandolare I e II
- Ipoparatiroidismo
- Artrite reumatoide
- Porpora trombocitopenica idiopatica (ITP)
- Diabete tipo II
- Anemia perniciosa
- Insufficienza surrenale
- Vitiligine
- Lupus sistemico eritematoso (SLE o Lupus)
- Osteoporosi
- malattie cardiache
- Tiroidite autoimmune
- Diabete tipo II
- Infertilità: solo il 5% delle pazienti POF di età <30 anni riesce ad avere una gravidanza spontanea.
- regime dietetico ipocalorico (1500-1700 KCal), ricco di fibre vegetali
- esercizio fisico regolare (aerobica e pesi)
- DHEA
- In caso di infertilità: COH (EE -DHEA- AI- HMG): Non esiste un trattamento efficace per ripristinare la fertilità in una donna affetta da SOR. Tentativi terapeutici prevedono cicli di iperstimolazione ovarica controllata (Controlled Ovarian Hyperstimulation, COH) utilizzando alte dosi di gonadotropine (HMG da preferire a r-FSH) e pre-trattamnento con estro-progestinici sono stati coronati da un basso indice (pregnancy rate/cycle 2-10%) di gravidanza (29). Inserire DHEA nel protocollo di stimolazione ovarica è giustificato dal notevole decremento di tale ormone nelle pazienti POF e dall’osservazione che un ambiente “androgenico” intraovarico PCO-simile favorirebbe il reclutamento di follicoli antrali suscettibili di maturazione. In tale ottica è giustificato il ricorso agli inibitori dell’aromatasi di terza generazione (Letrozolo, Femara©) da utilizzare nei primi giorni del ciclo. In caso di fallimenti ripetuti occorre giocoforza ricorrere all’ovodonazione, ovviamente all’estero grazie alla legge 40 e grazie agli Italiani che hanno votato contro il referendum per l’abrogazione di tale legge per incrementare il turismo sanitario e l’arricchimento dei centri clinici stranieri.
- AI (Assisted Insemination): è la tecnica da utilizzare in caso di oligospermia e/o ostilità cervicale.
- .FIVET/ICSI: in caso di oligoastenospermia e/o patologia tubarica.
- Ovodonazione nei Paesi in cui è consentita dalla legislazione vigente.
Senescenza ovarica precoce (Premature Ovarian Failure, POF), Menopausa precoce:
La menopausa precoce è la cessazione delle mestruazioni, con il suo corredo sintomatologico ed endocrinologico-metabolico, prima dei 40 anni di età (26). Escluse le cause chirurgiche, la menopausa precoce è dovuta a un esaurimento ovarico precoce (POF, Premature Ovarian Failure) con cui si identifica. Interessa circa l’1-4% della popolazione mondiale (27-43).
Sintomatologia e diagnosi POF:
- Amenorrea secondaria ipergonadotropa
- Metrorragie e menometrorragie
- E2: diminuisce in caso di POF. Valori sierici di E2 <30 pg/ml al 3° giorno del ciclo indicano una scarsa riserva ovarica; valori sierici di E2 <20 pg/ml indicano un totale esaurimento dell’attività follicolare ed una produzione di estradiolo in modo residuale; valori di E2 >50 pg/ml indicano la presenza di attività follicolare normale.
- Clomifene Challenge test negativo: dosaggio dei valori sierici di FSH al 3° giorno del ciclo; somministrazione di 100 mg di clomifene dal 5° al 9° giorno del ciclo; dosaggio FSH al 10° giorno. Il clomifene stimola la produzione di FSH. la crescita multifollicolare, la secrezione di estradiolo e l’aumento della β-inibina. Nelle donne fertili l’innalzamento della β-inibina provoca riabbassamento dei livelli sierici di FSH mentre nelle donne con ridotta riserva ovarica si ha un innalzamento della secrezione di FSH a cui però non segue una buona stimolazione ovarica, nè innalzamento dei livelli di estradiolo, secrezione di β-inibina e i livelli di FSH restano alti (64-66).
- SHBG (Sex Hormone Binding Globuline): diminuiscono in caso di POF. Sono sintetizzate a livello epatico; nella donna in età fertile i valori sierici normali sono 40-120 nmol/l. La sua sintesi è inibita da diete ipercaloriche ed iperlipidiche, ipotiroidismo, alti livelli di insulina, IGF-1 e androgeni ed invece stimolata da tiroxina, ipertiroidismo, Growth Hormone, estrogeni ed epatopatie. In pazienti in menopausa e POF diminuiscono nettamente al di sotto di 20 nmol/l. Una diminuzione significativa dell’SHBG comporta un aumento significativo dell’attività androgenica periferica (acne, virilismo, PCOS) ed una diminuzione dell’attività ovarica.
- DHEA: ormone prodotto dal surrene. Presenta valori sierici di 3-8
 ng/ml e diminuisce in caso di POF. Valori sierici <3 ng/ml indicano uno stato di insufficienza ovarica (46-51).
ng/ml e diminuisce in caso di POF. Valori sierici <3 ng/ml indicano uno stato di insufficienza ovarica (46-51). - Sindrome pre-mestruale
ETIOLOGIA POF:
- Idiopatica: le cause non sono identificabili nonostante ricerche mirate; comprende la quasi totalità dei casi
- Patologia ovarica autoimmune: causa distruzione del patrimonio follicolare ovarico e può essere distinta in:
- Auto-anticorpi anti-ovaio
- Sindrome polighiandolare autoimmune (61-64)
- Mutazione di geni specifici (Xfragile, INHA, FOXL2, ELF2B, BMP15, PMM2, AIRE)
- S. di de Giorge (Aplasia timica congenita)
3. Patologia ovarica iatrogena:
• chemioterapia: gli ovociti sono molto sensibili all’azione dei chemioterapici. Ogni mese di chemioterapia comporta una riduzione di 18 mesi di vita fertile.
• terapia radiante pelvica o “total body”
• terapia chirurgica: resezione cuneiforme eccessiva, cistectomia con eccessiva asportazione del parenchima ovarico, ovariectomia.
• virus della parotite epidemica: l’infiammazione delle gonadi se cronicizza provoca ne provoca la perdita della funzionalità.
4. Stress psico-fisici
5. Post-abortiva: Flamigni riporta tre casi di ovaio resistente, insorti dopo aborto spontaneo e regrediti spontaneamente e che hanno avuto gravidanze spontanee e mette in guardia dal fare prognosi negative senza prima avere effettuato una biopsia ovarica.
6. Talassemia major ed emocromatosi conseguente a scarso utilizzo del ferro da deficit di sintesi dell’eme o da eccessivo accumulo di ferro dopo trasfusioni. L’emocromatosi è molto più frequente negli uomini che nelle donne, ma in menopausa la differenza fra i due sessi si annulla per la cessazione delle mestruazioni, gravidanze e allattamenti. L’accumulo di ferro a livello gonadico induce disfunzionalità ovarica (come anche per tiroide, pancreas, fegato, cuore e cervello) e quindi ipogonadismo.
7. Galattosemia: l’incapacità di metabolizzare il galattosio è responsabile dell’insorgenza della POF presente nell’81% delle pazienti affette da galattosemia (67-70).
8. Fumo: le donne fumatrici sono a rischio di menopusa precoce. Sono alcune sostanze chimiche, i cosiddetti idrocarburi aromatici policiclici (PAHs) principalmente contenuti nel fumo di sigarette, che, dopo essersi legate a un particolare recettore (Ahr), attivano un gene (Bax) in grado di arrecare disturbi alla gametogenesi (69).
9. Inquinamento ambientale: emissioni di fossil fuel, alcuni tipi di scarichi industriali e solventi contenenti 2-bromopropane possono provocare menopausa precoce non per mancanza di follicoli ma per alterazione della loro funzionalità o per alterazione dei siti recettoriali ovarici per le gonadotropine.
10. Alcoolismo, Disordini alimentari, BMI <20 e BMI >35: il consumo di alcool danneggia il fegato e conseguentemente diminuisce la secrezione di SHBG con aumento dei livelli sierici di androgeni liberi.
TERAPIA:
Pillola estro-progestinica in combinazione fissa: .estrogeni e progestinici in associazione e in dosaggi fissi per 21,22,24 gg con intervalli rispettivamente di 7,6 e 4 giorni fra una confezione e l’altra: Yasminelle 21 cpr, Estinette 21 cpr, Lybella 21 cpr, Miranova 21 cpr, Harmonet 21 cpr, Loette 21 cpr. Alcune specialità commerciali, per semplificare, presentano blister di 28 cpr ma le ultime 4 pillole sono placebo; ovviamente non richiedono intervalli fra una confezione e l’altra: Drospil 28 cpr, Yaz 28 cpr, Alcmena 28 cpr, Arianna 28 cpr, Minesse 28 cpr.
Pillola estro-progestinica in combinazione sequenziale: estrogeni e progestinici sono combinati in dosaggi che cercano di mimare le variazioni sieriche del ciclo naturale, Più precisamente lo schema di assunzione prevederà l’incremento delle concentrazioni di etinilestradiolo durante la metà del ciclo per poi ridiscendere, ed un aumento graduale delle quantità del progestinico fino a fine ciclo. Tali variazioni, che sembrano ricalcare in parte quelle del normale equilibrio ormonale endogeno, dovrebbero, grazie anche all’utilizzo di progestinici innovativi come il gestodene, ridurre alcuni effetti collaterali importanti come gli spotting emorragici. Prodotti commerciali: Milvane 21 cpr, Triminulet 21 cpr, Gracial 22 cpr, Dueva 22 cpr, Klaira 28 cpr (79-81).
- DHEA 25 mg x 3/die: stesse indicazioni della S. di Savage (46-51)
- vitamina E (Evion cpr 50 mg): si trova soprattutto negli oli vegetali, nelle verdure e nei cereali integrali.
- Cortisonici: nelle forme autoimmuni la terapia immunosoppressiva corticosteroidea é di scarso ausilio ai fini del ripristino della fertilità (44, 45).
- SSRI (Selective Serotonin Reuptake Inhibitors): limitano i disturbi comportamentali
- COH e FIVET/ICSI: in caso di desiderio di gravidanza e grave deplezione follicolare
- Ovodonazione
- Crioconservazione del tessuto ovarico: può essere utilizzato nelle giovani donne a rischio di POF
la PCO che è responsabile del 75 % dei casi di amenorrea da anovulazione cronica.
TERAPIA:
La stimolazione ovarica per induzione dell’ovulazione e ripristino delle condizioni ormonali necessarie per il ripristino del flusso mestruale può essere ottenuta con:
-
- Gn-RH somministrato ev/sc con microinfusore; stimola direttamente l’ipofisi ad un’ipersecrezione di gonadotropine
- Gondotropine esogene che stimolano direttamente le ovaie
- Clomifene citrato (CC) che stimola indirettamente l’ipofisi e l’ipotalamo.
Il clomifene è un composto non steroideo simile al dietilstilbestrolo con attività essenzialmente antiestrogenica e debolmente estrogenica. Il suo meccanismo d’azione consiste in:
1) competizione recettoriale con gli estrogeni endogeni con effetti antiestrogenici su utero, mammella e vagina.
2) depressione del feed–back positivo degli estrogeni su ipotalamo e ipofisi che percepiscono un falso segnale di ipoestrogenismo e di conseguenza attivano un’ipersecrezione di GnRH e di gonadotropine.
NEOPLASIE OVARICHE ORMONO-SECERNENTI:
Si tratta di neoplasie molto rare che interessano meno del 3% delle neoplasie ovariche.
- Gonadoblastoma: amenorrea primaria e, più raramente, oligoamenorrea e amenorrea secondaria, anomalie cromosomiche (X0/XY); si associa frequentemente ad altre neoplasie ovariche
- Ginandroblastoma: metrorragia ed amenorrea
- Tumori a cellule della granulosa: iperestrogenismo che causa menometrorragie alternate a periodi di oligo-amenorrea, ipersecrezione di muco cervicale, aumento di volume dell’utero accrescimento precoce; nelle donne in pre-menopausa si nota un anomalo trofismo vaginale.
- Struma ovarico è composto completamente da tessuto tiroideo maturo. Possono produrre ipertiroidismo ed amenorrea.
- Tumori a cellule di Setoli-Leydig (arrenoblastomi): ipersecrezione di ormoni androgeni, irsutismo, virilismo, alopecia, diminuzione del volume mammario, menometrorragie ed amenorrea
La diagnosi del ca. ovarico è quasi sempre tardiva poiché il I° stadio (con prognosi di guaribilità che si aggira su 85-95%) rappresenta circa il 20% nelle casistiche più vaste.
I sintomi iniziali più comuni del ca. ovarico sono:
- dolore pelvico (57%)
- aumento di volume dell’addome (51%)
- metrorragia (25%)
- Amenorrea (5%)
- Androstenedione >30 nmol/L
- Estradiolo >300 pg/ml.
La terapia è basata su:
- rimozione delle neoplasie maligne,
- somministrazione di farmaci derivati dall’ergotamina in caso di microadenoma lattotropo
- terapia ormonale sostitutiva
AMENORREA DA PATOLOGIA ADENOIPOFISARIA
 AMENORREA DA PATOLOGIA IPOTALAMICA –L’amenorrea ipotalamica rappresenta la più comune forma di amenorrea da cause centrali con una frequenza del 20-40% di tutte le forme di amenorrea. L’amenorrea ipotalamica assume un’enorme importanza dal punto di vista clinico non soltanto per la condizione di infertilità, ma anche, e soprattutto, per alcune condizioni patologiche conseguenti allo stato di anovularietà e conseguente ipoestrogenismo con tutte le patologie del climaterio.
AMENORREA DA PATOLOGIA IPOTALAMICA –L’amenorrea ipotalamica rappresenta la più comune forma di amenorrea da cause centrali con una frequenza del 20-40% di tutte le forme di amenorrea. L’amenorrea ipotalamica assume un’enorme importanza dal punto di vista clinico non soltanto per la condizione di infertilità, ma anche, e soprattutto, per alcune condizioni patologiche conseguenti allo stato di anovularietà e conseguente ipoestrogenismo con tutte le patologie del climaterio.
 SINDROME DI SHERMAN: amenorrea ed ipomenorrea conseguente a terapia contraccettiva estro-progestinica prolungata.
SINDROME DI SHERMAN: amenorrea ed ipomenorrea conseguente a terapia contraccettiva estro-progestinica prolungata.
Amenorrea primaria da alterata produzione di Gn-RH congenito:
- Sindrome di Kallmann
- Sindrome di Prader-Willi
- Sindrome di Laurence-Moon-Biedl
- Ipogonadismo ipogonadotropo isolato
- Resistenza recettoriale al Gn-RH
- Mutazione DAX-1
a) Alterata produzione funzionale di Gn-RH:
- da stress, lutto: eventi stressanti di natura psicologica quali un lutto o una separazione, stalking, mobbing, insoddisfazioni lavorative, relazione difficoltosa con il partner.
- anoressia,
- dieta eccessivamente ipocalorica,
- eccesso di sport, danza: esercizio fisico intenso e/o di livello agonistico, con maggiore incidenza negli sport di resistenza o in quelli che richiedono una ridotta massa grassa corporea quali l’atletica leggera, il balletto, il pattinaggio artistico, etc.
- lutto
c) Danno anatomico acquisito:
- Craniofaringioma
- Germinoma
- Glioma
- Sindrome di Hand-Schuller-Christian
- Malattie granulomatose
- Radioterapia del cranio
- Traumi cranici
- Encefaliti
DIAGNOSI: Il momento fondamentale dell’iter diagnostico dell’amenorrea ipotalamica è rappresentato dall’anamnesi iniziale. Alla raccolta di un’anamnesi patologica prossima e remota completa ed accurata deve necessariamente accompagnarsi la scrupolosa raccolta dei dati riguardanti la storia mestruale e ginecologica della paziente precedente l’insorgenza della amenorrea, nonché la valutazione delle abitudini alimentari (dieta, abbuffate, etc.) dell’attività fisica svolta (tipo di sport, numero di ore settimanali di allenamento, etc.), degli eventi stressanti di tipo maggiore e/o minore, del consumo di farmaci e/o di sostanze stupefacenti. La possibile presenza di disturbi del comportamento alimentare, del tono dell’umore, etc., anche di tipo “borderline”, andrebbe esclusa e non si devono trascurare le caratteristiche cognitive e relazionali della paziente, il suo grado di soddisfazione per il lavoro e/o le attività svolte con particolare attenzione alle capacità di adattamento agli eventi stressanti della vita quotidiana. L’amenorrea ipotalamica rappresenta sostanzialmente una diagnosi di esclusione. Andranno pertanto escluse tutte le patologie endocrine considerate come possibile causa di anovularietà: iperprolattinemia, distiroidismi, alterazioni surrenaliche, e/o la presenza di malattie sistemiche.
I dosaggi ormonali basali dovrebbero comprendere le gonadotropine, il 17-β-estradiolo (E2), la prolattina (PRL), l’ormone tireo-stimolante (TSH), le frazioni libere degli ormoni tiroidei (fT3 ed fT4), indicatori della funzione androgenica ovarica (Androstenedione, A), surrenalica (deidroepiandrosterone, DHEA) e un indice di stress cronico (cortisolo). E’ utile, soprattutto ai fini di una maggiore motivazione alla terapia, l’esecuzione di una mineralometria ossea per la determinazione del contenuto calcico. L’ecografia pelvica è indicata come ausilio nell’esclusione di patologie ovariche che possono causare amenorrea secondaria.
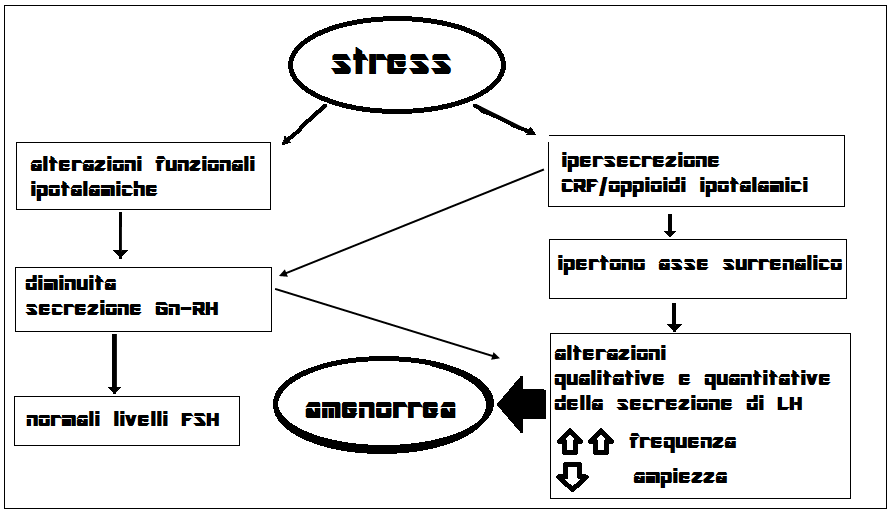
Alterazioni ormonali: Alla cessazione dell’attività pulsatile del GnRH ipotalamico, che causa quiescenza ovarica e il conseguente stato di ipoestrogenismo, si associano numerose alterazioni endocrine. Le più frequenti sono rappresentate da:
- ridotta ampiezza e/o frequenza della secrezione pulsatile delle gonadotropine ipofisarie, in particolare dell’LH, con valori bassi (generalmente inferiori a 3 UI/L);
- ipotiroidismo ipotalamico, spesso subclinico, con valori normali o ridotti della frazione libera degli ormoni tiroidei;
- ipercortisolemia per conseguenza dell’attivazione aspecifica dell’asse ipotalamo-ipofisi-surrenalico
- ipertono oppioide endogeno
- ipoinsulinemia
- ipotiroidismo ipotalamico
Dal punto di vista clinico non esistono segni e/o sintomi caratteristici di tale patologia, ove si eccettui la cessazione della normale ciclicità mestruale, insorta da almeno 6 mesi, ed, eventualmente, l’associazione con basso peso corporeo e basso indice di massa corporea (<19 (v.n. 21-24)).
TERAPIA: l’amenorrea secondaria ipotalamica, data la complessità e l’eterogenità dei fattori coinvolti, necessita di un approccio multidimensionale,  non soltanto di tipo endocrino-ginecologico. La terapia sarà adeguata alle esigenze della paziente. Nel caso di un immediato desiderio di gravidanza l’obiettivo primario sarà quello di ripristinare l’ovulazione e tale scopo può essere raggiunto mediante adeguati protocolli di stimolazione ovarica con gonadotropine o con somministrazione esogena di Gn-RH pulsatile im/sc a mezzo di apposito microinfusore. Nel caso le esigenze riproduttive non siano immediate, sono indicati schemi di terapia estrogenica sostitutiva e/o estro-progestinica.
non soltanto di tipo endocrino-ginecologico. La terapia sarà adeguata alle esigenze della paziente. Nel caso di un immediato desiderio di gravidanza l’obiettivo primario sarà quello di ripristinare l’ovulazione e tale scopo può essere raggiunto mediante adeguati protocolli di stimolazione ovarica con gonadotropine o con somministrazione esogena di Gn-RH pulsatile im/sc a mezzo di apposito microinfusore. Nel caso le esigenze riproduttive non siano immediate, sono indicati schemi di terapia estrogenica sostitutiva e/o estro-progestinica.
Consigli anti-stress:
- Mangiare a orari regolari
- Jogging: l’esercizio fisico non farà scomparire lo stress, ma ridurrà l’intensità emotiva percepita
- reflessologia plantare
- praticare un hobby
- aiutare persone in difficoltà: aiutare gli altri, per esempio attraverso il volontariato, è un efficace stimolo in grado di aumentare la resilienza; fornire supporto a persone che si trovano in problemi più grossi aiuta ad affrontare i propri con la giusta prospettiva, facendoti acquisire consapevolezza e serenità.
- rispettare i ritmi naturali
- Verdure crude
- ridurre caffè, tè, coca-cola, alcool
- barretta di cioccolato fondente
- massaggio taoista
- respirazione addominale
- battere le palpebre
- scrivere un diario
- accetta quello che non puoi cambiare e concentrati su quello che puoi realizzare
Distiroidismo – Nell’ipotiroidismo l’amenorrea potrebbe essere dovuta all’iperprolattinemia causata dallo stimolo da parte del TRH sulle cellule lattotrope.
Nell’ipertiroidismo i tassi estrogenici sono sempre elevati con alterazione dei meccanismi di feed-back. LH è alto con FSH normale e si determina così una condizione simile a quella della policistosi ovarica con amenorrea ed anovulazione.
Sindrome di di George o microdelezione del cromosoma 21q11.2:
è una delle poche malattie da carenza immunitaria da deficit da  linfociti T descritta per la prima volta nel 1960 dall’endocrinologo Angelo di George. I sintomi si manifestano subito dopo la nascita, determinata da un difetto embrio-morfogenetico. La patogenesi di questa rara patologia è da riferire a delezione del cromosoma 21q11.2 o mutazione del gene TBX1. I pazienti presentano ipoplasia o aplasia del timo e delle paratiroidi, con la caratteristica sintomatologia ipocalcemica (tetania, convulsioni) che si verifica nelle prime 24 ore di vita, malformazioni cardiache con difetti settali e interruzione dell’arco aortico e mancata chiusura del dotto arterioso, basso impianto auricolare, ipoplasia mandibolare, palatoschisi e labbro leporino. L’ipocalcemia di questi soggetti è permanente. Questa sindrome causa l’insorgenza di infezioni spesso letali. In un piccolo numero di casi è indicato il trapianto di timo fetale il più presto possibile e l’ipoparatiroidismo va curato con calcio al quale si deve aggiungere vitamina D o paratormone. Nel 30% dei casi sono presenti anomalie del sistema genito-urinario con amenorrea primaria o, più raramente, secondaria (76-78).
linfociti T descritta per la prima volta nel 1960 dall’endocrinologo Angelo di George. I sintomi si manifestano subito dopo la nascita, determinata da un difetto embrio-morfogenetico. La patogenesi di questa rara patologia è da riferire a delezione del cromosoma 21q11.2 o mutazione del gene TBX1. I pazienti presentano ipoplasia o aplasia del timo e delle paratiroidi, con la caratteristica sintomatologia ipocalcemica (tetania, convulsioni) che si verifica nelle prime 24 ore di vita, malformazioni cardiache con difetti settali e interruzione dell’arco aortico e mancata chiusura del dotto arterioso, basso impianto auricolare, ipoplasia mandibolare, palatoschisi e labbro leporino. L’ipocalcemia di questi soggetti è permanente. Questa sindrome causa l’insorgenza di infezioni spesso letali. In un piccolo numero di casi è indicato il trapianto di timo fetale il più presto possibile e l’ipoparatiroidismo va curato con calcio al quale si deve aggiungere vitamina D o paratormone. Nel 30% dei casi sono presenti anomalie del sistema genito-urinario con amenorrea primaria o, più raramente, secondaria (76-78).
List references:
- Dewhurts: Trattato di Ostetricia e Ginecologia. EMSI editore, 2012
- Massouras HG, Coutifaris B, Kalogirou D.: “Management of uterine adhesions with ‘Massouras Duck’s Foot’ and ‘Butterfly’ IUDs”. Contracept Deliv Syst.1982 Jan;3(1):25-38.
- S. Saraf; P. Saraf (2007). McIndoe Vaginoplasty: Revisited. The Internet Journal of Gynecology and Obstetrics 6(2).
- Vecchietti G (1965). [Creation of an artificial vagina in Rokitansky-Küster-Hauser syndrome]. Attual Ostet Ginecol 11 (2): 131–47 (in Italian). PMID 5319813.
- ^ Fedele L, Bianchi S, Tozzi L, Borruto F, Vignali M (1996). A new laparoscopic procedure for creation of a neovagina in Mayer-Rokitansky-Kuster-Hauser syndrome. Fertil. Steril. 66 (5): 854–7
- K. Morcel, D. Guerrier, T. Watrin, I. Pellerin, and J. Levêque, “The Mayer-Rokitansky-Küster-Hauser (MRKH) syndrome: clinical description and genetics,” Journal de Gynecologie Obstetrique et Biologie de la Reproduction, vol. 37, no. 6, pp. 539–546, 2008.
- J. E. Griffin, C. Edwards, and J. D. Madden, “Congenital absence of the vagina. The Mayer-Rokitansky-Küster-Hauser syndrome,” Annals of Internal Medicine, vol. 85, no. 2, pp. 224–236, 1976.
- K. Fisher, R. H. Esham, and I. Thorneycroft, “Scoliosis associated with typical Mayer-Rokitansky-Küster-Hauser syndrome,” Southern Medical Journal, vol. 93, no. 2, pp. 243–246, 2000. View at Scopus
- A. Pizzo, A. Fattori, C. Dugo, M. T. Mastroeni, C. Moscheo, and N. Dugo, “Syndrome of Rokitansky-Kunster-Hauser-Mayer: a description of four cases,” Minerva Ginecologica, vol. 59, no. 1, p. 95, 2007. View at Scopus
- E. H. Strübbe, C. W. Cremers, W. N. Willemsen, R. Rolland, and C. J. Thijn, “The Mayer-Rokitansky-Küster-Hauser (MRKH) syndrome without and with associated features: two separate entities?” Clinical Dysmorphology, vol. 3, no. 3, pp. 192–199, 1994. View at Scopus
- E. H. Strübbe, J. A. Lemmens, C. J. Thijn, W. N. Willemsen, and B. S. van Toors, “Spinal abnormalities and the atypical form of the Mayer-Rokitansky-Küster-Hauser syndrome,” Skeletal Radiology, vol. 21, no. 7, pp. 459–462, 1992. View at Scopus
- Schenker JG, Margalioth EJ. Intra-uterine adhesions: an updated appraisal. Fertility Sterility 1982; 37:593-610.
- V. Volpicelli, N. Lauda, L. Scotto Di Tella, V. Maisto, P. Laurino, A.A. Ferrari: “IVG: complicanze precoci”. Atti Congresso Nazionale “Applicazione, applicabilità e prospettive della legge 194”, Genova 22-24 Maggio 1981; Cofese Edizioni, Palermo.
- V. Volpicelli, N. Lauda, L. Scotto Di Tella, V. Maisto, P. Laurino, A.A. Ferrari: “Variazioni tecniche originali al metodo Karman per I.V.G.”. Atti Congresso Nazionale “Applicazione, applicabilità e prospettive della legge 194”, Genova, 22-24 Maggio 1981; Cofese Edizioni, Palermo.
- Parent B, Barbot J, Dubuisson JB. Uterine synechiae (in French). Encyl Med Chir Gynecol 1988; 140A (Suppl): 10-12.
- Dalton VK, Saunders NA, Harris LH, Williams JA, Lebovic DI.Intrauterine adhesions after manual vacuum aspiration for early pregnancy failure. Fertil Steril. 2006; 85(6):1823.e1-3.
- Krolikowski A, Janowski K, Larsen JV. Asherman syndrome caused by schistosomiasis.Obstet Gynecol. 1995; 85(5 Pt 2):898-9.
- Choi-WW; Yoo-JY; Park-KC; Kim-KH: “LEOPARD syndrome with a new association of congenital corneal tumor, choristoma”. PEDIATRIC-DERMATOLOGY. MAR-APR 2003; 20 (2) : 158-160
- Baron J, Hyla R: “The syndrome of ovarian hypoplasia”. .Zentralbl Gynakol. 1976;98(24):1491
- Sivanesaratnam, V. (1986) Unexplained unilateral ab-sence of ovary and fallopian tube. European Journal of Obstetrics & Gynecology and Reproductive Biology, 22, 103-105. doi:10.1016/0028-2243(86)90096-1
- James, D.F., Barber, H.R. and Graber, E.A. (1970) Torsion of normal uterine adnexa in children. Report of three cases. Obstetrics & Gynecology, 35, 226-230.
- Sebastian, J.A., Baker, R.L. and Cordray, D. (1973) Asymptomatic infarction and separation of ovary and distal uterine tube. Obstetrics & Gynecology, 41, 531-535.
- Silva, P.D., Glasser, K.E. and Virata, R.L. (1995) Spontaneously acquired unilateral absence of the adnexa. A case report. Journal of Reproductive Medicine, 40, 63-64.
- Acien, P. (1997) Incidence of Mullerian defects in fertile and infertile women. Human Reproduction, 12, 1372- 1376.
- Haydardedeoglu, B., Simsek, E., Kilicdag, E.B., Tarim, E., Aslan, E. and Bagis, T. (2006) A case of unicornuate uterus with ipsilateral ovarian and renal agenesis. Fertil-ity and Sterility, 85, 750.e1-750.e4.
- Georgy, F.M. and Viechnicki, M.B. (1974) Absence of an ovary and uterine tube. Obstetrics & Gynecology, 44, 441- 442
- Paolo Beck-Peccozand Luca Persani : “premature ovarian failure”. Orphanet Journal of Rare Diseases 2006, 1:9
- Simpson JL, Rajkovic A: “Ovarian differentiation and gonadal failure”. Am J Med Genet 1999, 89:186-200.
- Goswami D, Conway GS: “Premature ovarian failure”. Hum Reprod Update 2005, 11:391-410.
- Sybert PV, McCauley E: Turner’s syndrome. N Engl J Med 2004, 351:1227-1238.
- Achermann JC, Ozisik G, Meeks JJ, Jameson JL: “Perspective: genetic causes of human reproductive diseases”. J. Clin Endocrinol Metab 2002, 87:2447-2454.
- Sherman SL: Premature ovarian failure in the fragile X syndrome. Am J Med Genet 2000, 97:189-194.
- Méduri G, Massin N, Guibourdenche J, Bachelot A, Fiori O, Kuttenn F, Misrahi M, Touraine P. 2007. “Serum anti-Müllerian hormone expression in women with premature ovarian failure.” Hum Reprod., 22(1):117-23.
- Blumenfeld, Z, 2007. “Letter to the Editor: Pregnancies in patients with POF gonadotropin stimulation and pretreatment with ethinyl estradiol.” Fertility and Sterility 88(3):763.
- Blumenfeld, Z, 2007. “Letter to the Editor: Pregnancies in patients with POF gonadotropin stimulation and pretreatment with ethinyl estradiol.” Fertility and Sterility 88(3):763.
- Kalantaridou SN, Nelson LM (2000). “Premature ovarian failure is not premature menopause”. Ann. N. Y. Acad. Sci.900: 393–402.
- Prakash, G. J.; Ravi Kanth, V. V.; Shelling, A. N.; Rozati, R.; Sujatha, M. (2010). “Mutational analysis of inhibin alpha gene revealed three novel variations in Indian women with premature ovarian failure”. Fertility and Sterility94 (1): 90.
- Blumenfeld Z, Halachmi S, Peretz BA, Shmuel Z, Golan D, Makler A and Brandes JM, 1993. “Premature ovarian failure–the prognostic application of autoimmunity on conception after ovulation induction.” Fertility and Sterility 59(4):750-5.
- Beck-Peccoz P, Persani L (2006). “Premature ovarian failure”. Orphanet J Rare Dis 1: 9. doi:10.1186/1750-1172-1-9.
- Buckler HM J Clin Endocrinol Metabol 72:116-124, 1991.
- Coulam CB, Adamson SC, Annegers JF. Incidence of premature ovarian failure. Obstet Gynecol., 1986; 67: 604-6
- Prakash, G. J.; Ravi Kanth, V. V.; Shelling, A. N.; Rozati, R.; Sujatha, M. (2010). “Mutational analysis of inhibin alpha gene revealed three novel variations in Indian women with premature ovarian failure”. Fertility and Sterility 94 (1): 90. doi:10.1016/j.fertnstert.2009.02.014. PMID 19324345
- Graziottin A.: “Sexuality, aging and chronic diseases: iatrogenic premature menopause in cancer survivors“. Schneider H.P.G (Ed.), Menopause: state of the art, Parthenon Publishing, London, pag. 408-415, 2003
- Corenblum B, Rowe T, Taylor PJ. High-dose, short-term glucocorticoids for the treatment of infertility resulting from premature ovarian failure. Fertil Steril., 1993; 59: 988-91
- Van Kasteren YM, Braat DDM, Hemrika DJ, Lambalk CB, Rekers-Mombarg LTM, Von Blomberg BME, Rekers-Mombarg LTM, Von Blomberg BME, Schoemaker JS. Corticosteroids do not influence ovarian responsiveness to gonadotropins in patients with premature ovarian failure: a randomized, placebo-controlled trial. Fertil Steril., 1999; 71: 90-95
- Gleicher N, Weghofer A, Barad DH (2010). “Dehydroepiandrosterone (DHEA) reduces embryo aneuploidy: direct evidence from preimplantation genetic screening (PGS)”. Reprod. Biol. Endocrinol. 8: 140. doi:10.1186/1477-7827-8-140. PMC 2992540. PMID 21067609. http://www.rbej.com/content/8//140.
- Casson PR, Linday MS, Pisarska MD, Carson SA, Buster JE: “Dehydroepiandrosterone supplementation augments ovarian stimulation in poor responders: a case series. Hum Reprod 2000, 15:2129-2132.
- Barad DH, Gleicher N: “Increased oocyte production after treatment with dehydroepiandrosterone. Fertil Steril 2005,84:756.e1-3.
- Barad D, Gleicher N: “Effect of dehydroepiandrosterone on oocyte and embryo yields, embryo grade and cell number in IVF. Hum Reprod 2006, 21:2845-2949.
- Barad D, Brill H, Gleicher N: Update on the use of dehydroepiandrosterone supplementation among women with diminished ovarian function. J Assist Reprod Genet 2007, 24:629-634.
- Casson PR, Santoro N, Elkind-Hirsch K, Carson SA, Hornsby PJ, Abraham G, Buster JE: “Postmenopausal dehyroepiandrosterone administration increases free insulin-like growth factor I and decreases high-density lipoprotein: a six-month trial”. Fertil Steril 1998, 70:107-110.
- Jan W. van der Steeg, Pieternel Steures, Marinus J. C. Eijkemans, J. Dik F. Habbema, Peter G. A. Hompes, Frank J. Broekmans, Peter X. J. M. Bouckaert, Patrick M. M. Bossuyt, Fulco van der Veen, and Ben W. J. Mol, on behalf of the Collaborative Effort for Clinical Evaluation in Reproductive Medicine (CECERM) Study Group: “Predictive Value and Clinical Impact of Basal Follicle- Stimulating Hormone in Subfertile, Ovulatory Women”. (J Clin Endocrinol Metab 92: 2163–2168, 2007)
- Broekmans FJ, Kwee J, Hendriks DJ, Mol BW, Lambalk CB.: “A systematic review of tests predicting ovarian reserve and IVF outcome”. Hum Reprod Update 2006;12:685-718.
- Bancsi LF, Broekmans FJ, Mol BW, Habbema JD, te Velde ER.: “Performance of basal follicle-stimulating hormone in the prediction of poor ovarian response and failure to become pregnant after in vitro fertilization: a meta-analysis”. Fertil Steril 2003;79:1091-100.
- Jain T, Soules MR, Collins JA.: “Comparison of basal follicle-stimulating hormone versus the clomiphene citrate challenge test for ovarian reserve screening”. Fertil Steril 2004;82:180-5
- Muttukrishna S, McGarrigle H, Wakim R, Khadum I, Ranieri DM, Serhal P.: “ Antral follicle count, anti-mullerian hormone and inhibin B: predictors of ovarian response in assisted reproductive technology?”. Bjog 2005;112:1384-90.
- Ebner T, Sommergruber M, Moser M, Shebl O, Schreier-Lechner E, Tews G.: “Basal level of anti-Mullerian hormone is associated with oocyte quality in stimulated cycles”. Hum Reprod 2006;21:2022-6.
- Min Hye Choi, Ji Hee Yoo, Hye Ok Kim, Sun Hwa Cha, Chan Woo Park, Kwang Moon Yang, In Ok Song, Mi Kyoung Koong, Inn Soo Kang.: “Serum anti-Müllerian hormone levels as a predictor of the ovarian response and IVF outcomes”. Clin Exp Reprod Med 2011;38(3):153-158
- Blazar AS, Lambert-Messerlian G, Hackett R, et al.:”Use of in-cycle antimüllerian hormone levels to predict cycle outcome”. Am J Obstet Gynecol, 2011;205:223.
- Gnoth C, Shuring AN, Frid K, Tigger J.: “Relevance of AMH measurement in a routine IVF program”. Hum Reprod, 2008;23:1359–65.
- Hoek A, Schoemaker J, Drexhage HA. Premature ovarian failure and ovarian autoimmunity. Endocr Rev, 1997; 18: 107-34
- La Barbera Ar, Miller MM, Ober C, Rebar RW. Autoimmune etiology in premature ovarian failure. Am J Reprod Immunol., 1988; 16: 115-22
- Sedmak DD, Hart WR, Tubbs RR. Autoimmune oophoritis: a histopathologic study of involved ovaries with immunologic characterization of the mononuclear cell infiltrate. Int J Gynecol Pathol, 1987; 6: 73-81
- Hendriks DJ, Broekmans FJ, Bancsi LF, de Jong FH, Looman CW, Te Velde ER. Repeated clomiphene citrate challenge testing in the prediction of outcome in IVF: a comparison with basal markers for ovarian reserve. Hum Reprod 2005;20:163-9.
- 35) Hendriks DJ, Mol BW, Bancsi LF, te Velde ER, Broekmans FJ. The clomiphene citrate challenge test for the prediction of poor ovarian response and nonpregnancy in patients undergoing in vitro fertilization: a systematic review. Fertil Steril 2006;86:807-18
- 36) Hendriks DJ, Mol BW, Bancsi LF, Te Velde ER, Broekmans FJ. Antral follicle count in the prediction of poor ovarian response and pregnancy after in vitro fertilization: a meta-analysis and comparison with basal follicle-stimulating hormone level. Fertil Steril 2005;83:291-301. 54.
- HL, Driscoll SG, Porensky RS, Wender DF. Ovarian Failure in galactosemia. N Engl J Med., 1984; 310-50
- Waggoner DD, Buist NRM, Donnel GN. Long-term prognosis in galactosemia: results of a survey of 350 cases. J Inherit Metab Dis., 1990; 13: 802-18.
- Sun L, Tan L, Yang F, Luo Y, Li X, Deng HW, Dvornyk V: “Meta-analysis suggests that smoking is associated with an increased risk of early natural menopause”. Menopause. 2011 Sep 19. [Epub ahead of print]
-
Berry GT: ” Galactosemia and amenorrhea in the adolescent. Ann N Y Acad Sci. 2008;1135:112-7. doi: 10.1196/annals.1429.038.
-
Massouras HG, Coutifaris B, Kalogirou D.; “Management of uterine adhesions with ‘Massouras Duck’s Foot’ and ‘Butterfly’ IUDs”. Contracept Deliv Syst. 1982 3,1:25-38.
- Umme Salma, Dabao Xu*, Md Sayed Ali Sheikh: “Observational study of new treatment proposal for severe intrauterine adhesion”. International Journal of Biosciences (IJB) ISSN: 2220-6655 (Print) Vol. 1, No. 1, p. 43-56, 2011
- Diamond MP. 2000. Incidence of postsurgical adhesions. In di Zerega G (Ed.). Peritoneal Surgery (Sprinter-Verlag, New York) pp, 217–20
- S. Jean. “Physical Examination of the Child and Adolescent” (2000) in Evaluation of the Sexually Abused Child: A Medical Textbook and Photographic Atlas, Second edition, Oxford University Press. 62
- Sally E. Perlman, Nakajima, Steven T. and Hertweck, S. Paige, Clinical protocols in pediatric and adolescent gynecology, Parthenon, 2004, p. 131.
- Caridad de las Mercedes Tablada Borrero. Síndrome de Di George (Aplasia o Hipoplasia tímica). Multimed 2011; 15(1).
- Fomin A, Pastorino AC, Kim Chong A, Pereira CA, Carneiro-Sampaio M, Abe-Jacob CM. DiGeorge Syndrome: a not so rare disease. Clinics [artículo en Internet]. 2010
- Di George AM. Congenital absence of the thymus and its immunological consequences: concurrence with congenital hypoparathyroidism. Birth Defects 1968; 4: 116-21.
- Lete I, Morales P.: Inhibition of follicular growth by two different oral contraceptives (monophasic and triphasic) containing ethinylestradiol and gestodene. Eur J Contracept Reprod Health Care. 1997 Sep;2(3):187-91.
- Coata G, Ventura F, Lombardini R, Ciuffetti G, Cosmi EV, Di Renzo GC. Effect of low-dose oral triphasic contraceptives on blood viscosity, coagulation and lipid metabolism. Contraception. 1995 Sep;52(3):151-7.
- Weber-Diehl F, Unger R, Lachnit U. Triphasic combination of ethinyl estradiol and gestodene. Long-term clinical trial. Contraception. 1992 Jul;46(1):19-27.












14 commenti
Hi there mates, its impressive paragraph about tutoringand entirely explained, keep it up all the time.
Really annoyed me however the doctor told me it’s
possible to treat it, not cure it under the right circumstances.
It’s amazing in support of me to have a site, which is useful in support
of my experience. thanks admin
Link exchange is nothing else however it is just placing the other person’s weblog
link on your page at suitable place and other person will also do similar in favor of you.
Thanks on your marvelous posting! I really enjoyed reading it,
you happen to be a great author. I will make sure to bookmark your blog and
definitely will come back in the future. I want to encourage you to definitely continue your
great work, have a nice weekend!
Excellent, what a weblog it is! This web site provides useful facts to us, keep
it up.
Simply wish to say your article is as amazing.
The clearness to your put up is just cool and i can think you’re
a professional on this subject. Well along with your permission let me to take hold of your feed to keep up to date
with impending post. Thank you a million and please continue the
gratifying work.
Have you ever thought about writing an ebook or guest authoring on other
sites? I have a blog based on the same information you discuss and would love to have you share some stories/information. I know my
readers would value your work. If you’re even remotely interested,
feel free to shoot me an e mail.
Wonderful goods from you, man. I have understand your stuff previous to and you are just extremely wonderful.
I really like what you have acquired here, really like what you’re
saying and the way in which you say it. You
make it entertaining and you still take care of to keep it sensible.
I can not wait to read much more from you. This
is really a wonderful web site.
Every weekend i used to go to see this web page, for the reason that i wish for
enjoyment, for the reason that this this website conations actually good funny stuff too.
Wow, wonderful blog layout! How long have you been blogging for?
you make blogging look easy. The overall look of your web
site is fantastic, as well as the content!
Hi there Dear, are you in fact visiting this site daily,
if so afterward you will without doubt get fastidious knowledge.
Hello, this weekend is nice for me, because this time i am reading this wonderful informative post here at my house.
Simply desire to say your article is as amazing. The clearness in your post is simply great
and i can assume you’re an expert on this
subject. Fine with your permission allow me to grab your feed
to keep updated with forthcoming post. Thanks a million and please keep up
the enjoyable work.