Ultimo aggiornamento 2023-03-24
OVULAZIONE:
L’ovulazione è un fenomeno che prevede la deiscenza dell’ovocita dal suo follicolo  sotto l’influenza di LH, inibina, PGF2α, fattori enzimatici e meccanici. Questo complesso evento si verifica normalmente a metà del ciclo mestruale nella donna in età fertile. E’ un evento fondamentale nel complesso meccanismo della riproduzione.
sotto l’influenza di LH, inibina, PGF2α, fattori enzimatici e meccanici. Questo complesso evento si verifica normalmente a metà del ciclo mestruale nella donna in età fertile. E’ un evento fondamentale nel complesso meccanismo della riproduzione.
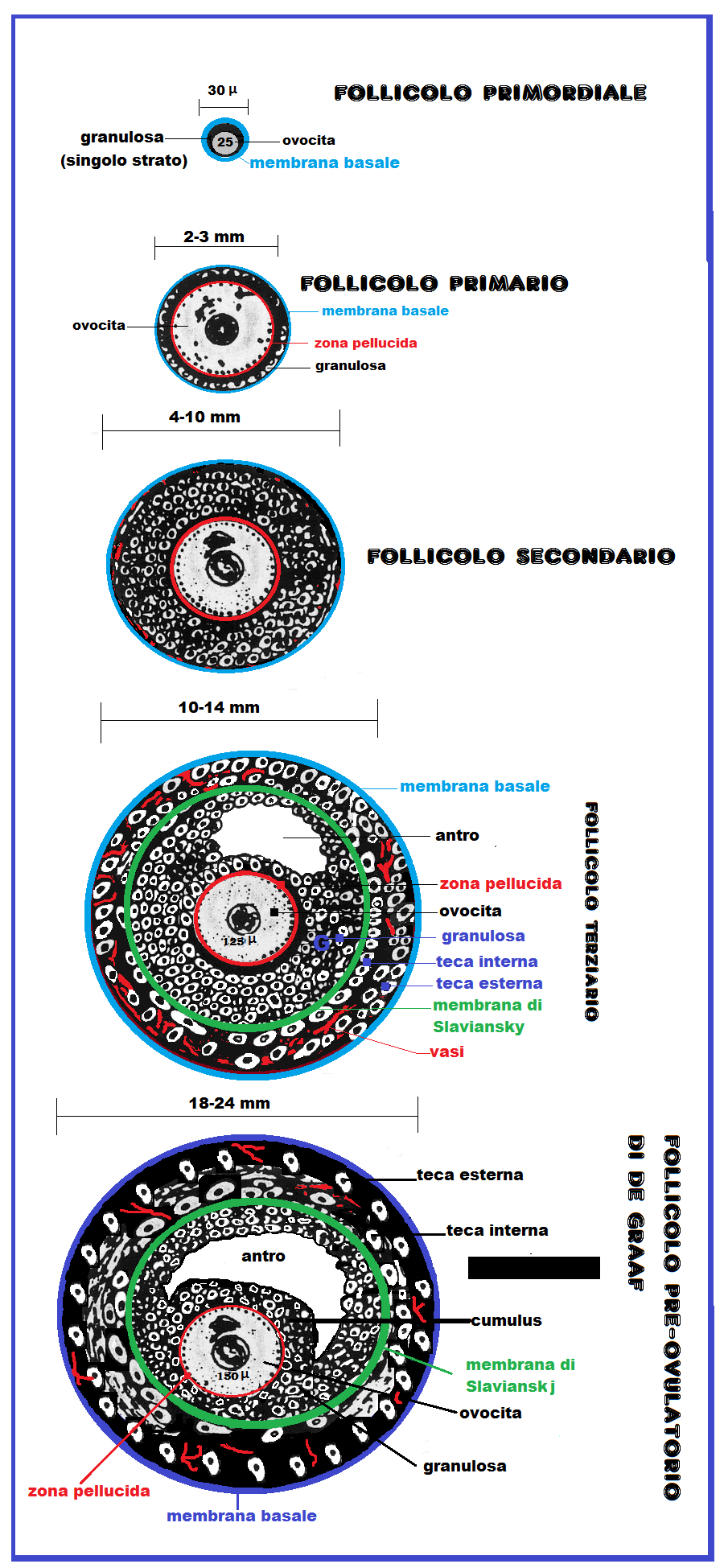
La formazione dei follicoli ovarici, che rappresentano strutturalmente la quota più cospicua e il compartimento funzionale più importante della corticale ovarica, inizia nel periodo embrionale, durante il quale si costituisce una riserva di cellule germinali: gli ovogoni. Questi vanno incontro a proliferazione mitotica che inizia dalla 4a settimana di gestazione e raggiunge l’acme alla 7a settimana quando i follicoli ovarici raggiungono il numero di 7.000.000 circa. Gli ovogoni si trasformano in ovociti primordiali del diametro di 25 µ bloccato nello stadio di profase della prima divisione meiotica. L’ovocita primordiale si circonda di un singolo strato di cellule della granulosa appiattite esternamente racchiuse da una membrana basale. Si formano così i follicoli primordiali con un diametro di 30 µ.
Dalla 7a settimana inizia la fase di degenerazione follicolare e morte cellulare per apoptosi che dalla 12a settimana non è più compensata dalla proliferazione mitotica e quindi il numero dei follicoli progressivamente diminuisce. Al momento della pubertà il patrimonio follicolare dell’ovaio é costituito da circa 300.000 follicoli primari. Questi ultimi, rispetto ai follicoli primordiali, sotto l’azione dell’FSH, presentano una trasformazione delle cellule della granulosa da pavimentose semplici in cubiche e da monostrato in pluristratificate (2-3 strati) raggiungendo un diametro totale di 2-3 mm. Inoltre sia la granulosa che l’ovocita primario secernono 4 glicoproteine (denominate ZP1, ZP2, ZP3 and ZP4) e microvilli (GAP junctions, giunzioni comunicanti). Le GAP sono giunzioni intermembranose costituite da una serie di canalicoli (o connessoni) del diametro di 2 nm e lunghi 7,5 nm che si aprono e chiudono con meccanismo a scatto in risposta a modificazione del pH o a variazioni delle concentrazione degli ioni calcio. Le gap junctions permettono il passaggio di ioni o molecole di basso peso molecolare (fino a 1 kDa) tra le cellule della granulosa e l’ovocita (4,5). Le gap junctions, le glicoproteine e uno strato di acqua interposte tra l’ovocita e le cellule della granulosa formano la zona pellucida o membrana vitellina che si frappone fra le membrane citoplasmatiche. La ZP ha un ruolo fondamentale nel processo di fecondazione prevenendo la polispermia e inducendo la reazione acrosomiale dello spermatozoo (5-11).
Fino alla pubertà, alla scansione ecografica si osserveranno solo follicoli primari del diametro di 2-3 mm. Di questi follicoli la maggior parte é destinata a scomparire per atresia mentre molti altri, sotto l’azione dell’FSH, si trasformeranno in follicoli secondari.
Nel follicolo secondario le cellule della granulosa subiscono un’ulteriore proliferazione in numero (3-6 strati) ed in grandezza ed iniziano la secrezione di liquido colloide formando piccoli spazi fra gli strati della granulosa (corpi di Call-Exner). Le cellule dello stroma connettivale dell’ovaio intervengono a far parte del follicolo, circondandolo a formare la teca follicolare.
Follicolo terziario: sotto l’influenza dell’FSH, alcuni follicoli secondari continuano la maturazione e si trasformano in follicoli terziari ma uno solo, il follicolo leader, riesce a completarla e raggiungere lo stadio IV° o di de Graaf. La selezione follicolare avviene al 5-7° giorno del ciclo. Il follicolo leader è quello che fortuitamente, o per maggiore sensibilità all’FSH, riceve maggiori quantità di FSH ed LH ed è quello che esprimerà più recettori per quest’ultime, ricevendo ancora ancor più gonadotropine instaurando un circolo vizioso a suo favore mentre gli altri follicoli vanno incontro ad una progressiva atresia pur avendo assunto una certa capacità steroidogenetica.Le cellule della granulosa continuano a proliferare soprattutto da un lato avvolgendo l’ovocita e andando a costituire il cumulo ooforo. La secrezione di liquido follicolare aumenta e l’antro è nettamente visibile ecograficamente. Le cellule tecali si dispongono in due strati: esterno (endocrinologicamente inerte) ed interno (ormono-secernenente). Le cellule tecali e quelle della granulosa sono separate dalla membrana di Slaviaskj.
Follicolo pre-ovulatorio di de Graaf: il follicolo va incontro a ulteriore maturazione e aumento di volume. Racchiuso nella sua membrana basale presenta dall’esterno all’interno un doppio strato di cellule tecali: esterne (non dotate di funzionalità steroidogenetica) e uno strato di cellule tecali interne deputate alla sintesi degli androgeni e del progesterone. Più internamente sono situate gli strati delle cellule della granulosa nettamente separate dalle cellule tecali dalla membrana di Slavianskj. I vasi sanguigni sinusoidali sono situati solo fra le cellule tecali e mai negli strati della granulosa. La cavità antrale occupa la parte centrale del follicolo e il liquido follicolare spinge sia l’ovocita che le cellule della granulosa verso la periferia; si viene così a formare il cumulo ooforo. Il follicolo è ormai maturo e viene chiamato follicolo di Graaf che raggiunge un diametro di 18-21 mm (range 16-24 mm) a causa dell’iperplasia delle cellule tecali e della granulosa e dell’abbondanza del liquido follicolare. L’ovocita, avvolto nella membrana detta membrana vitellina o zona pellucida, raggiunge le dimensioni definitive di 100-150 micron (0.1-0.15 mm).
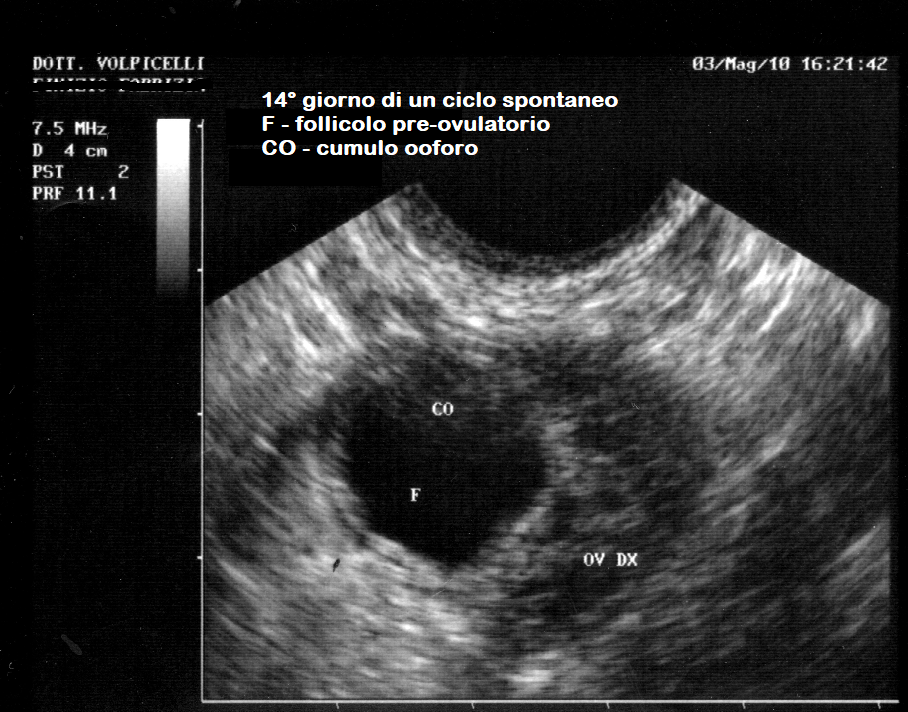 Nel follicolo pre-ovulatorio di de Graaf, sotto l’azione dell’LH, il cumulo ooforo si distacca dalla granulosa basale e va a posizionarsi all’estremità distale del follicolo. La sua apposizione sulla parete interna del follicolo determina una sporgenza a convessità esterna, lo stigma, dal quale uscirà l’ovocita.
Nel follicolo pre-ovulatorio di de Graaf, sotto l’azione dell’LH, il cumulo ooforo si distacca dalla granulosa basale e va a posizionarsi all’estremità distale del follicolo. La sua apposizione sulla parete interna del follicolo determina una sporgenza a convessità esterna, lo stigma, dal quale uscirà l’ovocita.
Quindi dei 7 milioni di follicoli presenti nell’ovaio fetale, solo 400-500, durante la vita riproduttiva della donna, andranno incontro alla completa maturazione ed alla ovulazione con liberazione di un ovocita maturo ad ogni ciclo. Tutti gli altri follicoli, il 99.9%, vanno in atresia e scompaiono per apoptosi.
Nei follicolo che giunge a maturità, l’ovocita, completate le ultime tappe del suo accrescimento, porta a termine la prima divisione meiotica (detta anche riduzionale), che, grazie ad una citodieresi asimmetrica, produce un il I° primo globulo polare e l’ovocita di 2° ordine nel quale il corredo cromosomico è ormai aploide. Dopodichè l’ovocita secondario inizia la meiosi II che però si arresta in metafase. Lo sblocco di queste due meiosi è dovuto alla neutralizzazione, da parte dell’ormone luteinizzante (LH), di un fattore inibente la meiosi prodotto dalle cellule del cumulo ooforo e reperibile nel liquido follicolare. Al momento della sua espulsione, l’oocita di 2° ordine è bloccato nella metafase della seconda divisione meiotica che potrà completarsi con la formazione dell’uovo maturo e l’emissione del II° globulo polare, solo se avrà luogo la fecondazione.
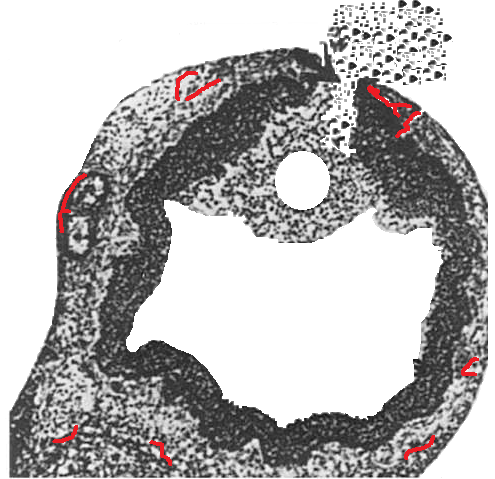
La rottura del follicolo: il meccanismo non è ancora completamente conosciuto ed è scarsamente studiato. Tra i fattori che determinano lo scoppio follicolare il principale risulta il surge dell’LH, che è all’apice della piramide delle reazioni a cascata che provocano lo scoppio del follicolo. Il surge dell’LH è determinato dall’aumentata secrezione di estradiolo che agisce con meccanismo di feed-back positivo su ipotalamo ed ipofisi (8-14). Sotto l’azione dell’LH, cAMP mediata, le cellule della granulosa, specialmente quello dello strato basale più ricco di recettori per LH (22,23), aumentano di volume e secernono maggiore quantità di liquido follicolare (costituito da acqua e mucopolisaccaridi), il cumulo ooforo si libera prima nel liquido follicolare e poi si avvicina alla parete distale del follicolo, si incunea nello spazio creato dalla degradazione enzimatica e forma sulla superficie esterna dell’ovaio un’estrusione rotondeggiante chiamata stigma. L’aumentata pressione endofollicolare era ritenuta la principale causa dello scoppio follicolare fino agli anni ’60. Il razionale di questa conclusione era basata sul rapido aumento del volume del liquido follicolare nelle ore precedenti la rottura follicolare. Successivamente si è dimostrato che la maggiore secrezione di liquido follicolare non sempre corrisponde ad una maggiore pressione endoluminale e che quest’ultima, ove fosse presente, gioca un ruolo secondario nel meccanismo dello scoppio follicolare (13-14).
Attualmente primaria importanza si attribuisce ad alcuni enzimi proteolitici come la plasmina, la collagenasi e le metalloproteinasi (24), la fosfatasi acida,i lisosomi, NO, i radicali liberi dell’ossigeno, leucociti e varie citochine (IL-1, EGF) che, attivati dall’LH, degradano il collagene della parete follicolare fino alla sua rottura permettendo la deiscenza dell’ovocita (14,15,21).
La prostaglandina PGF2α e l’angiotensina II stimolano la contrazione delle fibrocellule muscolari lisce perifollicolari e inducono vasocostrizione (calcio-mediata) delle arteriole perifollicolari. In particolare subiscono vasocostrizione e corrosione le arteriole situate nella zona dello stigma (14-19). La somministrazione di prostaglandina-sintetasi (indometacina) nel ratto inibisce lo scoppio del follicolo anche in presenza di LH-HCG (16-17).
Progesterone: fattore chiave dello scoppio follicolare. Antagonisti del progesterone, incluso RU 486, inducono riduzione o blocco dello scoppio follicolare. Le cellule della granulosa iniziano a secernere progesterone nei giorni precedenti il picco di LH, ma è immediatamente dopo il surge di LH che la produzione di progesterone da parte delle cellule della granulosa è massima
Sotto l’azione combinata di tutti questi fattori, il liquido follicolare e l’ovocita, circondato da alcune cellule del cumulo ooforo (che vanno a formare la corona radiata), viene espulso dall’ovaio.
Quindi i principali fattori attualmente conosciuti che determinano lo scoppio del follicolo sono;
- LH
- Progesterone
- PGF2α
- Angiotensina II
- Collagenasi
- Plasmina
- Metalloproteinasi
- fosfatasi acida
- lisosomi
- Citochine (Il-1, EGF)
- Leucociti
- Aumentata pressione intrafollicolare (?)
Le fimbrie tubariche, che nel periodo dell’ovulazione si sono avvicinate alle ovaie, catturano l’ovocita e lo spingono all’interno dell’ovidotto.
L’ovulazione può essere dimostrata solo ecograficamente quando si vede la  scomparsa del follicolo che nei giorni precedenti aveva raggiunto dimensioni maggiori di cieca 18-20 mm. In corso di laparoscopia è possibile osservare lo stigma; In rarissimi casi, con molta fortuna, si è potuto osservarsi un’ovulazione in diretta.
scomparsa del follicolo che nei giorni precedenti aveva raggiunto dimensioni maggiori di cieca 18-20 mm. In corso di laparoscopia è possibile osservare lo stigma; In rarissimi casi, con molta fortuna, si è potuto osservarsi un’ovulazione in diretta.
L’imminenza dell’ovulazione è segnalata, oltre che dai dosaggi ormonali e dalla scansione ecografica, dalla trasformazione del muco cervicale che  diventa abbondante, chiaro e filante con l’approsimarsi dell’ovulazione.
diventa abbondante, chiaro e filante con l’approsimarsi dell’ovulazione.
La filanza del muco cervicale (spinbarkeit) si misura ponendo una goccia del muco fra due vetrini e misurare la distanza che si riesce ad ottenere senza rompere il contatto; la distanza fra i due vetrini aumenta con l’approssimarsi dell’ovulazione.
Una goccia del muco cervicale strisciata su un vetrino mostrerà all’osservazione microscopica una tipica arborescenza “a foglia di felce” (fern-test) da attribuire alla cristallizzazione dei sali di sodio contenuti nel muco. Il grado di arborizzazione è espressa in gradi (I-II-III-IV) ed è strettamente correlata con la concentrazione plasmatica di 17-β-estradiolo.
sali di sodio contenuti nel muco. Il grado di arborizzazione è espressa in gradi (I-II-III-IV) ed è strettamente correlata con la concentrazione plasmatica di 17-β-estradiolo.
In genere dopo 24-36 ore dall’acme di queste caratteristiche del muco si verifica l’ovulazione.
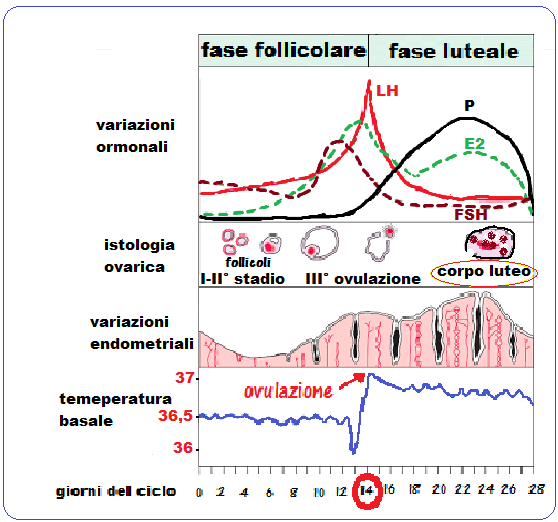
Altro segno indiretto dell’ovulazione è dato dalla curva della temperatura basale che, rispetto alla media della temperatura in fase follicolare, presenta un picco di +1 °C in corrispondenza dell’ovulazione, e quindi in fase luteale si assesta su un plateau costante di -0.5 °C rispetto al picco ovulatorio (v. grafico successivo).
Steroidogenesi follicolare: L’ovaio, stimolato da FSH ed LH, produce tutte e tre le classi di steroidi sessuali: estrogeni, progestinici e androgeni ma in differenti percentuali rispetto al testicolo a causa della diversità di enzimi critici. L’ovaio si differenzia dal corticosurrene perchè manca sia della 21-β-idrossilasi che della 11-β-idrossilasi e pertanto non può produrre glicocorticoidi e mineralcorticoidi (1,2). Oltre agli androgeni, E2 e P nel follicolo ovarico sono sintetizzati β-inibina, attivina, IGF I, IGF II, TGF, AMH.
FSH: è responsabile della
- proliferazione delle cellule della granulosa
- secrezione del liquido follicolare
- secrezione dell’estradiolo (stimolando l’aromatasi)
- induzione dei recettori per LH nel follicolo antrale
- proliferazione dei recettori per FSH
- secrezione dell’aromatasi
- secrezione di inibina
Il calo della concentrazioni di FSH all’8° giorno circa del ciclo mestruale svolge un ruolo importante nella selezione del follicolo dominante. La secrezione di FSH in declino all’8° giorno circa previene lo sviluppo follicolare multiplo, in quanto solo il follicolo leader rimane al di sopra della soglia (threshold) di FSH perchè ha il maggior numero di recettori FSH e può continuare a svilupparsi mentre gli altri follicoli passano in atresia per insufficiente stimolazione FSH. I recettori FSH scompaiono dal follicolo nella fase pre-ovulatoria.
LH:
- azione antimitotica: ostacola o arresta la proliferazione mitotica delle cellule della granulosa.
- permette la captazione endocellulare del colesterolo mediante stimolazione della proteina ART.
- stimola la secrezione di testosterone, androstenedione e progesterone tecali.
- determina la maturazione finale dell’ovocita, ottimale secrezione di estradiolo e abilità alla rottura della parete follicolare. Nei cicli PMA/FIVET è possibile ottenere follicoli maturi con la somministrazione del solo FSH ma i follicoli così cresciuti, senza LH, possono presentarsi di scadente qualità con bassa percentuale di fertilizzazione e pregnancy rate.
- promuove la dissoluzione del complesso cumulus-ovocita
- trigger dell’ovulazione promuovendo l’attivazione degli enzimi litici
- luteinizzazione delle cellule della granulosa
- Sblocco della meiosi
- permette la formazione e sopravvivenza del corpo luteo
- permette la produzione del progesterone da parte delle cellule luteali.
Durante la fase iniziale e middle-folliolare la secrezione di LH è modesta con picchi di secrezione ogni 60-90 minuti. Il picco della secrezione di LH si osserva al 10-11° giorno del ciclo ed è determinato dall’aumentata secrezione degli estrogeni che mediante feed-back positivo stimolano ipotalamo e direttamente l’adenoipofisi a produrre maggiori quanità di LH. L’ovulazione avviene approssimativamente 10-12 ore dopo il picco di LH e 24-36 ore dopo il picco follicolare di estradiolo.
Quindi le due gonadotropine agiscono in sincronia e contemporaneamente ma in concentrazioni diverse e su cellule distinte. Ciò ha indotto molti AA. a formulare la teoria delle 2 cellule 2 gonadotropine.
Il follicolo dominante acquisisce un’elevata capacità steroidogenetica con picco al 12º giorno e cioè 36-48 ore prima dell’ovulazione.
Estradiolo (E2): è il più importante dei tre estrogeni presenti in circolo. E’ secreto dalla cellule della granulosa per trasformazione degli androgeni ad opera dell’aromatasi (CYP 19) sotto l’influenza dell’FSH. Raggiunge un picco di 150-300 pg/ml al 9-10° giorno del ciclo per declinare rapidamente poco prima del picco LH. In fase middle-luteale l’estradiolo presenta un nuovo modesto rialzo dovuto all’attività delle cellule luteali. Funzioni dell’E2 nel processo ovulatorio:
- stimola la crescita follicolare in sinergia con l’FSH
- stimola la filanza e la quantità del muco cervicale
- Stimola la secrezione del liquido antrale.
- stimola la secrezione ipofisaria di LH mediante feed-back positivo sia a livello ipotalamico che direttamente sull’adenoipofisi
- deprime la secrezione di FSH con meccanismo di feed-back negativo a livello ipofisario
I livelli di E2 precipitano alcune ore dopo che l’LH ha raggiunto il suo picco per poi risalire in fase middle-luteale ed in fase pre-mestruale.
Estrone (E1): prodotto al 50% dalla granulosa, al 30% dal surrene per metabolizzazione del DHEA e al 20% a livello del tessuto adiposo per conversione dagli androgeni. In ogni caso agisce l’enzima aromatasi (CYP 19), L’E1 Ha un’emivita molto breve e possiede un’efficacia funzionale pari al 30% dell’E2. La sua maggiore produzione percentuale si verifica nei follicoli primari e secondari e quindi è il principale componente della concentrazione ematica iperestrogenica delle pazienti PCO.
Estriolo (E3): funzionalmente è il più debole dei 3 estrogeni, è il risultato della metabolizzazione di estradiolo ed estrone a livello epatico e placentare (3).
Androgeni: favoriscono la crescita follicolare in sinergia dell’FSH. Ma in assenza di FSH determinano atresia follicolare. L’aromatasi permette la metabolizzazione degli androgeni in estrogeni.
AMH: la secrezione di AMH è più alta nei follicoli primari, diminuisce e quindi si arresta nel momento in cui i follicoli si ingrandiscono. Non vi è quasi AMH nei follicoli umani >8 mm. Per questi motivi, i livelli sono quasi costanti ed il test AMH può essere fatto in qualsiasi giorno del ciclo della donna. Con l’aumento dell’età femminile la dimensione dell’insieme dei follicoli microscopici rimanenti, diminuisce. Allo stesso modo, diminuiscono i loro livelli ematici di AMH ed il numero dei follicoli ovarici antrali visibili con ecografia. Donne con molti piccoli follicoli, come coloro con ovaie policistiche hanno alti valori dell’ormone AMH e donne che hanno pochi follicoli rimanenti e coloro che sono vicine alla menopausa hanno bassi livelli di ormone antimulleriano.
Prolattina: la prolattina influenza indirettamente la funzione ovarica modulando la secrezione delle gonadotropine. La presenza di recettori specifici sulle cellule della granulosa del follicolo di de Graaf evidenzia incontestabilmente un ruolo diretto della PRL esercita sull’ovulazione ma il meccanismo è ancora sconosciuto (20).
L’ovulazione di norma avviene quindi dopo uno sviluppo follicolare durato circa 14 giorni e ad essa segue la trasformazione delle cellule della granulosa in cellule luteiniche e la luteinizzazione anche delle cellule della teca (cellule teco-luteiniche). Si ha così la formazione del corpo luteo che ha un’attività steroidogenetica caratterizzata dalla prevalete secrezione del progesterone su quella degli estrogeni. Se non si verifica la fecondazione la vita del corpo luteo dura solo 14 giorni, ma già dopo una settimana la sua attività comincia a declinare perché i livelli crescenti di progesterone e di estrogeni, che il corpo luteo ha prodotto in fase di massima attività, inducono a livello ipofisario e ipotalamico, per un feed back inibitorio o negativo, una progressiva depressione dei livelli di Gn-RH, LH, FSH e, di conseguenza, la funzione luteinica tende ad esaurirs e le cellule muoiono per apoptosi.
Se si verifica la fecondazione e, quindi, si instaura la gravidanza, il trofoblasto embrionale incomincia a produrre precocemente sempre più elevate quantità di gonadotropina corionica (HCG, Human Chorionic Gonadotropin), ad azione simile all’LH ipofisario. In questo caso non si ha più il declino funzionale del corpo luteo che anzi aumenta la sua efficienza e diventa corpo luteo gravidico, persistendo per qualche mese nella sua attività. Se la fecondazione non c’é stata, al declino funzionale del corpo luteo (con la rapida caduta dei livelli ematici di progesterone e di estrogeni), consegue lo sfaldamento della mucosa uterina: la mestruazione.
ANOVULAZIONE
L’assenza dell’ovulazione può dipendere da varie cause: alcuni farmaci (antineoplastici), insufficienza ormonale, contraccezione orale. L’induzione artificiale dell’ovulazione, tramite la somministrazione di FSH e LH purificati, fa parte del trattamento di alcune forme di sterilità. La mancata ovulazione non si traduce necessariamente in amenorrea.
ATRESIA FOLLICOLARE:
Il processo di atresia è caratterizzata da:
- degenerazione delle cellule della granulosa e morte geneticamente programmata per apoptosi che vengono rimpiazzate da fibroblasti;
- riassorbimento del liquido antrale con obliterazione della cavità antrale;
- sostituzione dei componenti situati all’interno della lamina basale con tessuto cicatriziale e avascolare con formazione dei cosiddetti corpi albicanti.
- Contemporaneamente le cellule tecali da prima si ipertrofizzano, successivamente si differenziano e ridiventono cellule interstiziali. Queste cellule conservano una debole attività steroidogenetica, soprattutto per quanto riguarda la produzione di androgeni .
Compiti del follicolo atresico:
- A parte il dissolvimento degli ovociti nei follicoli che non vanno incontro all’ovulazione, il ruolo funzionale dell’atresia nell’ovaio non è ben chiaro.
- Durante le prime fasi della pubertà, prima della comparsa dei cicli ovulatori, i follicoli destinati all’atresia sono in grado di produrre estrogeni, importanti per lo sviluppo dei caratteri sessuali secondari.
Il processo atresico sembra essere regolato dagli androgeni ed in particolare dalla frazione 5-alfa-ridotta, non aromatizzabile.
Bibliografia:
- Erickson GF: “An analysis of follicle develop,emt and ovum maturation”. Seminars Repeod Endocrinol; 1986 4:233
- Hillier SG, Reichert LE jr, Van Hall EV: “Control of preovulatory follicular estrogen biosyntesis in the human ovary”. J Clin Endocrinol Metab; 1981;52:847
- Barney Kadis: “Estriol Biosynthesis by Sow Ovary” Biochemistry, 1964, 3 (12), pp 2016–2019
- Gupta SK1, Bhandari B, Shrestha A, Biswal BK, Palaniappan C, Malhotra SS, Gupta N.: “Mammalian zona pellucida glycoproteins: structure and function during fertilization”. Cell Tissue Res. 2012 Sep;349(3):665-78.
- Gupta SK, Bansal P, Ganguly A, Bhandari B, Chakrabarti K.: “Human zona pellucida glycoproteins: functional relevance during fertilization”.J Reprod Immunol. 2009 Dec; 83(1-2):50-5. Epub 2009 Oct 21.
- Gupta SK, Chakravarty S, Suraj K, Bansal P, Ganguly A, Jain MK, Bhandari B.Structural and functional attributes of zona pellucida glycoproteins.Soc Reprod Fertil Suppl. 2007; 63:203-16.
- Omidi M et al: “zona pellucida and meiotic spindle visualitation of human oocytes are not influenced by in vitro maturation tecnology”. Intern J Fertik and steril 2013;7,S1:35-36
- Michal Margalit a, Gedalia Paz a, Haim Yavetz a, Leah Yogev a, Ami Amit a, Tamar Hevlin-Schwartz a,Satish K. Gupta b, Sandra E. Kleiman: “Genetic and physiological study of morphologically abnormal human zona pellucida”. European J Obstet Gynecol Reprod Biol 2012; 165:70–76
- Lefievre L, Conner SJ, Salpekar A, et al. Four zona pellucida glycoproteins are expressed in the human. Human Reproduction 2004;19:1580–616.
- Conner SJ, Lefievre L, Hughes DC, Barratt CL. Cracking the egg: increased complexity in the human zona pellucida. Human Reproduction 2005;5:1148–52.
- Wassarman PM. Mammalian fertilization: molecular aspects of gamete adhesion, exocytosis and fusion. Cell 1999;96:175–83.
- LeMaire WJ “Mechanism of mammalian ovulation”. Steroids. 1989 Nov;54(5):455-69.
- Morioka N, Zhu C, Brännström M, Woessner JF, LeMaire WJ.: “Mechanism of mammalian ovulation”. Prog Clin Biol Res. 1989; 294:65-85.
- Okamura H.: “Control mechanism of ovarian function”. Nihon Sanka Fujinka Gakkai Zasshi: 1991 Aug; 43(8):890-6.
- Cajander S, Bjersing L: Fine structural demonstration of acid phosphatase in rabbit germinal epithelium prior to induced ovulation. Cell Tissue Res 164: 179, 1975
- Yoshimura Y, Santulli R, Atlas SJ et al: The effects of proteolytic enzymes on in vitro ovulation in the rabbit. Am J Obstet Gynecol 157: 468, 1987
- Edward E. Wallach: “The Mechanism of Ovulation”. online 2013
- Diaz-Infante A Jr, Wright KH, Wallach EE: Effects of indomethacin and prostaglandin F2α on ovulation and ovarian contractility in the rabbit. Prostaglandins 5: 567, 1974
- Wallach EE, de la Cruz A, Hunt J et al: The effect of indomethacin on HMG-HCG induced ovulation in the indomethacin-treated Rhesus monkey. Prostaglandins 9: 645, 1975
- Hamada Y et al:Inhibitory effect of prolactin on ovulation in the in vitro perfused rabbit ovary. Nature 285: 15, 1980
- Cajander S, Bjersing L: Fine structural demonstration of acid phosphatase in rabbit germinal epithelium prior to induced ovulation. Cell Tissue Res 164: 179, 1975
- Hum. Reprod. Update (2007) 13 (3): 289-312.
- Bortolussi M,Marini G,Reolon ML. A histochemical study of the binding of 125I-HCG to the rat ovary throughout the estrous cycle. Cell Tissue Res1979;197:213-26.
- Brannstrom M, Woessner JFJ, Koos RD,et al. Inhibitors of mammalian tissue collagenase and metalloproteinases suppress ovulation in the perfused rat ovary. Endocrinology1988;122:1715-21.
- Brannstrom M, Pascoe V, Norman RJ, et al . Localization of leukocyte subsets in the follicle wall and in the corpus luteum throughout the human menstrual cycle. Fertil Steril 1994;61:488-95.









11 commenti
Fantastic post however , I was wanting to know if you could write a litte more on this subject?
I’d be very grateful if you could elaborate a little bit more.
Appreciate it!
When some one searches for his essential thing, so he/she desires to be available that in detail, so
that thing is maintained over here.
Link exchange is nothing else however it is just placing the other
person’s blog link on your page at appropriate
place and other person will also do similar in support of you.
Wonderful web site. Plenty of useful info here.
I’m sending it to a few pals ans also sharing in delicious.
And certainly, thanks in your sweat!
I am actually glad to glance at this weblog posts which includes
tons of valuable information, thanks for providing such data.
It’s going to be ending of mine day, but before end I am reading this enormous
post to improve my knowledge.
Hello, I enjoy reading through your article. I wanted to write a little
comment to support you.
Thank You! Cheers
I’m impressed, I have to admit. Seldom do I come across a blog that’s both educative and interesting, and without a doubt,
you’ve hit the nail on the head. The problem is something too few folks are speaking intelligently about.
I’m very happy I stumbled across this during my hunt for
something regarding this.
Very nice article, just what I needed.
A motivating discussion is worth comment. There’s no doubt that that
you should write more on this topic, it might not
be a taboo matter but usually folks don’t discuss these
topics. To the next! Best wishes!!