Ultimo aggiornamento 14/01/2025
TUMORI OVARICI BORDERLINE
Definizione
I tumori ovarici borderline (BOT) sono caratterizzati da una proliferazione cellulare ed atipia nucleare epiteliale in assenza di invasione stromale o diffusione peritoneale (se l’invasione peritoneale è presente, dovrebbe essere non distruttiva e inferiore a 5 mm in dimensioni lineari). Rappresentano una forma intermedia fra il cistadenoma e l’adenocarcinoma. Alcuni BOT hanno una forma minore di invasione designato come microinvasione; altri presentano piccole aree focali che mostrano da moderata a grave atipie cellulari (stratificazione epiteliale, perdita della polarità, atipie nucleari, architettura cribriforme mitosi occasionali) che sono designati come carcinomi intraepiteliali. Nel 1929 furono descritti per la prima volta da Taylor che li definì semimaligni. Attualmente costituiscono un capitolo controverso nell’ambito della patologia neoplastica dell’ovaio. Non vi è, infatti, a tutt’oggi, un accordo tra i patologi riguardo il loro inquadramento nosologico. Il termine borderline esprime un concetto nebuloso e rimane indefinito nel suo comportamento biologico benigno o potenzialmente maligno. La proposta di classificazione di Kurman (1) prevede, pertanto, l’abolizione del termine borderline almeno per i tumori sierosi e mucinosi dell’ovaio e la loro riclassificazione (v. tabella seguente). Studi recenti hanno suggerito che la presenza o l’assenza di micropapillarità e la presenza o assenza di diffusione peritoneale possano essere caratteristiche affidabili per una classificazione dei BOT in tumori benigni e maligni (8). McCluggage ritene che la presenza di grave atipia nucleare in un tumore ovarico sieroso, anche in assenza di invasione, è sufficiente per diagnosticare il tumore come carcinoma sieroso di alta qualità (11).
Etiologia: non chiara
Frequenza: 15% di tutti i tumori epiteliali ovarici (5)
Prognosi: La sopravvivenza per i tumori allo stadio I è praticamente al 100%
Fattori di rischio:
- Età alla prima gravidanza
- fumo
- Anamnesi familare positiva per cancro ovarico
Di solito si presentano ad un’età media inferiore rispetto all’età di presentazione dei tumori ovarici maligni ed in genere vengono diagnosticati a stadi precoci ed hanno una buona prognosi ma possono dare origine a tumori epiteliali decisamente maligni.
ISTOLOGIA: macroscopicamente i tumori ovarici borderline sono simili ai cistoadenomi sierosi: appaiono di dimenioni aumentata (10-15 cm in media con ampio range di oscillazione), di consistenza teso-elastica, a superficie liscia di colore variabile dal rosa al rosso e al marrone in caso di stravaso emorraggico interno, con capsula tesa, riccamente vascolarizzata e con aree di ispessimento.
Alla sezione ovarica Il tumore può presentarsi uni- o multiloculato.
Formazioni papillari esuberanti possono evidenziarsi sulla superficie esterna della cisti o nel suo lume. Le strutture papillari sono generalmente di colore giallo-marrone; sono fragili, con una minima stratificazione epiteliale e coperte da liquido sieroso, marrone o mucinoso e spesso sono collegate fra di loro “a ponte”. La presenza delle papile serve a distinguere il TBL sieroso dal cistadenofibroma. Il 69% dei TBL che presentano una componente papillare sulla superficie esterna sono associati con impianti peritoneali rispetto al 16% dei casi in cui la papillarità è soltanto intracistica (10).
Le papille possono presentare gruppi di cellule che si estroflettono e si “tuffano” nel liquido cistico (“tufting“). Il tufting è il risultato di gruppi indipendenti di cellule epiteliali dalle punte delle papille, per mancanza di sostegno tessuto connettivo. Talvolta queste formazioni si uniscono fra di loro creando una formazione “a rosetta”.
Il liquido contentuto nella cisti può essere di un colore giallo paglierino, emorragico o mucinoso denso. Il contenuto mucinoso non indica necessariamente che il tumore sia di tipo mucinoso.
La porzione ovarica residua libera dal tumore può essere difficile da individuare, soprattutto quando il tumore è molto grande.
I TBL istologicamente possono essere divisi, in base alle caratteristiche epiteliali (cellule epiteliali basse o cellule epiteliali alte mucinose), in sierosi (91%), mucinosi (3%), endometrioidi (2%), a cellule chiare (2%) e tumori di Brenner (2%). I tumori borderline dell’ovaio sono bilaterali nel 30% dei casi e si associano ad impianti extra-ovarici nel 35% dei casi.
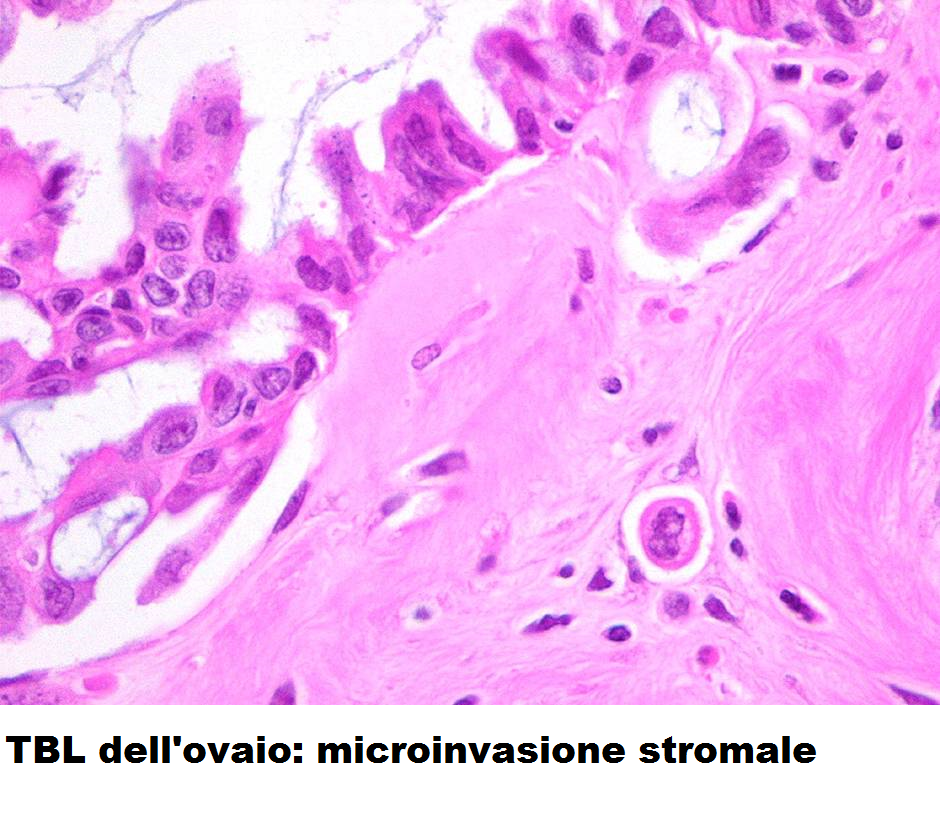
Almeno 2 sezioni o più devono essere esaminate per ogni centimetro della lesione tumorale (9). In caso di atipie cellulari, occorre allargare l’esame istologico anche nelle zone apparentemente sane (12). Le atipie cellulari nei TBL dovrebbero essere di grado intermedio, Tuttavia, ci sono aree di TBL che mostrano i cambiamenti pari a un carcinoma intraepiteliale (stratificazione epiteliale, perdita della polarità, atipie nucleari, architettura cribriforme e mitosi occasionali). Questo tipo di lesione è ora classificato come microcarcinoma a basso grado non invasivo (13-15). Invasività: < 5 mm (16).
Diagnosi
Questi tumori, così come gli altri tumori ovarici, sono difficili da individuare clinicamente finché non arrivano ad uno stadio avanzato o raggiungono dimensioni notevoli. Il sintomo più comune è il dolore addominale, la crescita della circonferenza dell’addome, la tensione addominale, disuria, dispareunia. Il 23% delle pazienti è asintomatica.
USG: L’ecografia pelvica transvaginale con color Doppler può essere utile pre-operatoriamente per valutare la possibile malignità della massa, anche se l’esame non si dimostra molto sensibile e specifico.
Stadiazione; La stadiazione del tumore rappresenta uno dei fattori più importanti nella decisione della terapia da intraprendere e consiste nell’esplorazione della cavità addominale, nell’aspirazione del liquido peritoneale o nel lavaggio con il prelievo di un campione, nell’omentectomia, nella rimozione di lesioni peritoneali sospette e nell’esecuzione di biopsie multiple del peritoneo.
Tumore di Brenner: raro tumore dell’ovaio (1.2% di tutti i tumori ovarici), benigno nel 95% dei casi, a lenta evoluzione. È una forma molto rara che deriva da residui embrionali, Si ritrova in genere nelle donne di età >40 anni e più frequentemente in post-menopausa. Si accresce molto lentamente, senza provocare sintomi caratteristici e può raggiungere volumi molto variabili: 3-30 cm. Quando è di piccole dimensioni è asintomatico. Se di dimensioni maggiori, i sintomi non sono specifici. Alla palpazione addominale si apprezza come una massa a limiti netti, ci consistenza teso-cistica, localizzata in zona annessiale. All’esame TAC in zona annessiale si evidenzia come una formazione espansiva, rotondeggiante , del diametro max di 3-30 cm, a prevalente contenuto liquido e a pareti ispessite ove si possono osservare gettoni solidi, in parte calcifici, di verosimile significato eterologo.
Non recidiva dopo l’asportazione chirurgica e solo in casi molto rari si ha un’evoluzione maligna.
Istologia è caratteristica: le cellule sono di tipo misto epitelio-stromale di derivazione dall’urotelio embrionale immerso in stroma ovarico denso. Anche le cavità cistiche maggiori sono rivestite dallo stesso tipo di epitelio. Presenza di focolai di epitelio muciparo e di microcalcificazioni distrofiche. Presenza di aree di proliferazione epiteliale e di atipia nucleare. Assenza di aspetti invasivi. Il liquido contenuto nella cisti è di colore giallo-citrino.
Terapia:
La risposta ad un trattamento ormonale nei carcinomi di basso grado è superiore rispetto al trattamento chemioterapico, mentre la percentuale di stabilità di malattia è sovrapponibile nei due gruppi di trattamento. Le terapie ormonali utilizzate nel carcinoma mammario (tamoxifene, letrozolo, anastrozolo) presentano tutte attività nel carcinoma ovarico di basso grado (2).
Le nuove possibilità terapeutiche per le pazienti con recidiva di malattia sono caratterizzate da molecole ‘target’, cioè con un bersaglio molecolare ben definito, come il Selumetinib (AZD6244) – inibitore di MEK (MAPK/ERK kinase) e che ha dimostrato una risposta maggiore (15%) rispetto alla chemioterapia convenzionale (5%) e all’ormonoterapia (7-8%) ed ha ottenuto il 65% di stabilizzazione di malattia.
Le pazienti con uno stadio 1 del tumore vengono sottoposte a trattamento conservativo che consiste nella cistectomia o salpingo-ovariectomia monolaterale (6).
Il follow-up postoperatorio è molto importante dal momento che le recidive possono presentarsi anche molti anni dopo il trattamento (7). Le recidive crescono in media di 1 mm al mese, permettendo il follow-up delle pazienti per lunghi periodi.
Nel caso in cui il tumore interessi entrambe le ovaia o quando il tumore si sviluppa in una paziente precedentemente ovariectomizzata o quando il tumore è ad uno stadio avanzato la paziente viene sottoposta a chirurgia radicale: washing peritoneale, isterectomia totale, annessiectomia bilaterale, omentectomia, resezione delle lesioni peritoneali macroscopiche e biopsie multiple del peritoneo. Nei primi due anni dopo l’intervento si consigliano controlli ogni tre mesi e dal terzo al quinto anno il follow up deve essere eseguito ogni sei mesi. Durante il controllo si esegue l’esame obiettivo, l’ecografia transvaginale e la valutazione del CA-125 (1,8).
- Mentre può essere considerato opportuno un atteggiamento di attesa vigile anche di fronte a masse annessiali di una certa dimensione (6-10 cm) in donne in età premenopausale e con valori di Ca125 normali o non particolarmente alti, la maggior parte delle masse ovariche nelle donne in età postmenopausale richiederà una valutazione chirurgica.
- E’ comunque da sottolineare che nonostante esista una notevole varietà di parametri clinici, di laboratorio e di diagnostica per immagini, nessuna combinazione di questi fattori può considerarsi accurata al 100% nel predire la presenza di un processo neoplastico maligno in particolar modo nella diagnostica delle lesioni allo stadio iniziale (3).
Bibliografia:
-
Mirjam J.A. Engelen, M.D.Henk W.A. de Bruijn, Ph.D. et al: “Serum CA 125, Carcinoembryonic Antigen, and CA 19-9 as Tumor Markers in Borderline Ovarian Tumors”.Gynecologic Oncology July 2000 Volume 78, Issue 1, Pages 16–20
- Pecorelli S et al. Massa pelvica: diagnosi e terapia. Collana di ginecologia e ostetricia nella prati-
ca clinica. Milano: Paletto Editore, 1996.
-
J. Chambers,M J. Merino, E.I. Kohorn, P.E. Schwaerz: “Borderline ovarian tumors”.American Journal of Obstetrics and Gynecology Volume 159, Issue 5, November 1988, Pages 1088–1094
-
Skírnisdóttir I, Garmo H, Wilander E, Holmberg L. Borderline ovarian tumors in Sweden 1960-2005: trends in incidence and age at diagnosis compared to ovarian cancer. Int J Cancer. Oct 15 2008;123(8):1897-901.
-
Cadron I, Leunen K, Van Gorp T, Amant F, Neven P, Vergote I. Management of borderline ovarian neoplasms. J Clin Oncol. Jul 10 2007;25(20):2928-37Seidaman JD, Cho KR, Ronnett BM, Kraus RJ. Surface Epithelial Tumors of the Ovary, In Blaustein’s Pathology of the female genital tract, Chapter 14, Six Edition, Springer, New York, 2011
-
Romeo M, Pons F, Barretina P, Radua J. Incomplete staging surgery as a major predictor of relapse of borderline ovarian tumor. World J Surg Oncol. Jan 23 2013;11:13
-
Seidman JD1, Kurman RJ. Ovarian serous borderline tumors: a critical review of the literature with emphasis on prognostic indicators. Hum Pathol. 2000 May;31(5):539-57.
-
Seidaman JD, Cho KR, Ronnett BM, Kraus RJ. Surface Epithelial Tumors of the Ovary, In Blaustein’s Pathology of the female genital tract, Chapter 14, Six Edition, Springer, New York, 2011
- Longacre, T.A., R.L. Kempson, and M.R. Hendrickson, Well-differentiated serous neoplasms of the ovary. Pathology (Phila), 1993. 1(2): p. 255-306.
- McCluggage WG: The pathology of and controversial aspects of ovarian borderline tumours. Curr Opin Oncol. 2010 Sep;22(5):462-72.
- Dietel, M. and S. Hauptmann, Serous tumors of low malignant potential of the ovary. 1. Diagnostic pathology. Virchows Arch, 2000. 436(5): p. 403-12.
- Hart WR, Ovarian epithelial tumors of borderline malignancy (carcinomas of low malignant potential). Hum Pathol, 1977. 8(5): p. 541-9.
- Riman, T., et al., Risk factors for epithelial borderline ovarian tumors: results of a Swedish case-control study. Gynecol Oncol, 2001. 83(3): p. 575-85.
- Modugno, F., R.B. Ness, and J.E. Wheeler, Reproductive risk factors for epithelial ovarian cancer according to histologic type and invasiveness. Ann Epidemiol, 2001. 11(8): p. 568-74.
- McKenney JK, Balzer BL, Longacre TA: Patterns of stromal invasion in ovarian serous tumors of low malignant potential(borderline tumors): a reevaluation of the concept of stromal microinvasion. Am J Surg Pathol. 2006 Oct;30(10):1209-21.









1 commento
magnificent publish, ery informative. I ponder whhy thhe
other experts off thyis secctor don’t relize this. You
should continue yyour writing. I aam confident, yyou have a great readers’ base
already!