Ultimo aggiornamento 05/08/2024
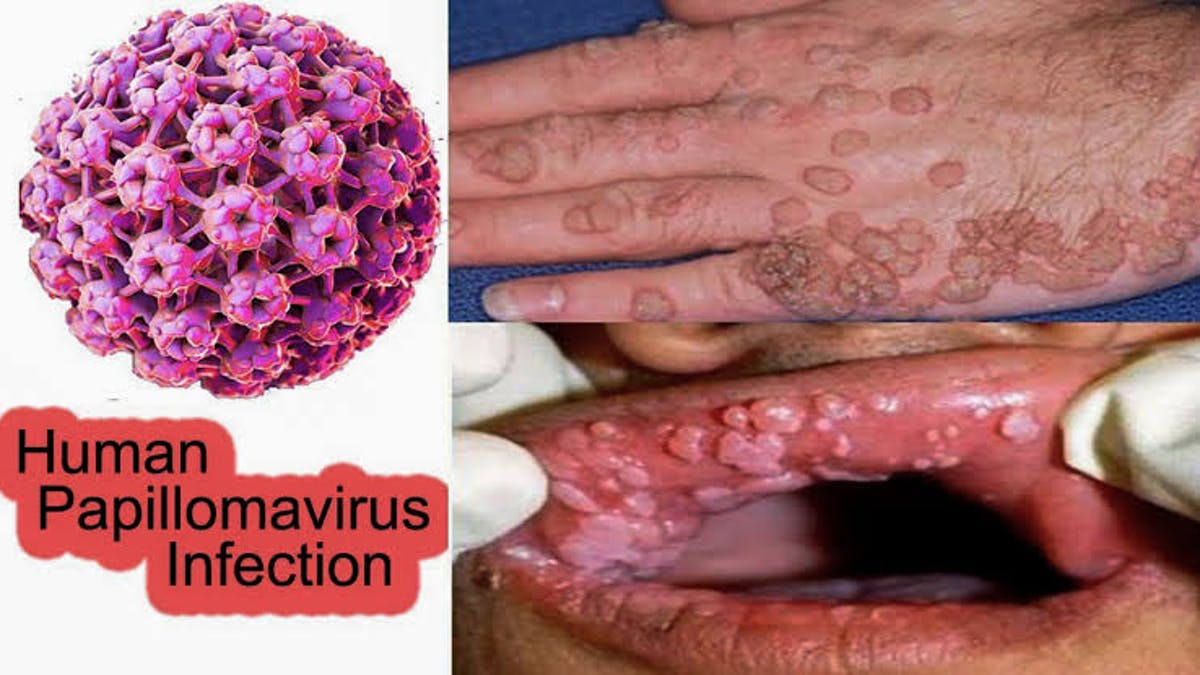
Nell’ambito delle infezioni ginecologiche, quelle da virus del papilloma (HPV) rivestono particolare importanza, per l’aumentata frequenza (incremento del 700% negli anni 60-80), per i loro stretti rapporti con i tumori del basso tratto della sfera genitale femminile, per la multifocalità delle lesioni genitali indotte, per la latenza subclinica e infine per le modalità di contagio.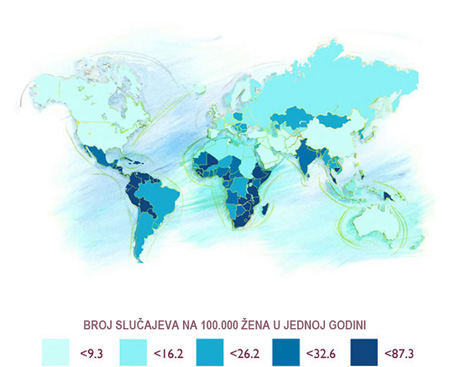
Il tessuto epiteliale squamoso, che ricopre la cute e le cavità comunicanti con l’esterno (come la mucosa vaginale e la bocca), è l’ospite naturale per l’attecchimento e la replicazione del virus HPV.
In particolare la zona cervicale di giunzione squamo-colonnare è particolarmente sensibile all’infezione da HPV perchè sprovvista di uno strato di cellule inattive; inoltre l’epitelio colonnare endocervicale è composto da un singolo strato cellulare.
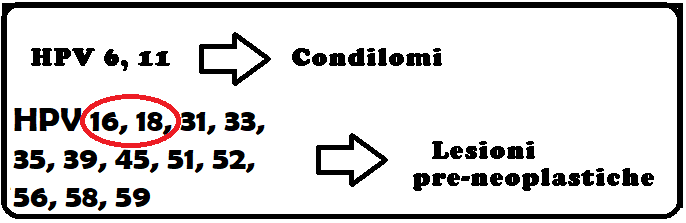
Sintomatologia: I sintomi variano in base al tipo di infezione. Generalmente, i segni più comuni dell’infezione sono le verruche (verruche comuni, verruche plantari, verruche genitali) da riferire ad infezioni da parte di HPV a basso rischio (6 e 11). Le verruche a localizzazione genitale vengono definite condilomi e possono riscontrarsi sui genitali esterni, sulla mucosa vaginale, anale e perineale. Queste 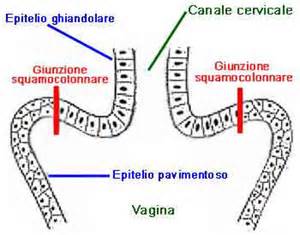 lesioni si manifestano come piccole escrescenze, a volte disposte a grappolo, dalla forma che ricorda quella di un cavolfiore (condilomi acuminati).
lesioni si manifestano come piccole escrescenze, a volte disposte a grappolo, dalla forma che ricorda quella di un cavolfiore (condilomi acuminati).
In altri casi le lesioni sono piatte (condilomi piani) e tendono a sovrapporsi (9-11).
La maggior parte delle lesioni causate da HPV sono asintomatiche, ma in alcuni casi, le verruche possono provocare fastidio, prurito o disagio. 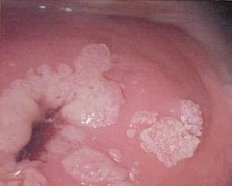
La maggior parte delle infezioni genitali da HPV regredisce spontaneamente. Una piccola quota invece, se non trattata, può evolvere lentamente verso una forma tumorale. Il ca. cervicale è infatti quasi sempre correlato alla presenza dell’HPV. La deviazione neoplastica in genere è lenta; sono necessari circa 10-15 anni prima che l’infezione da HPV, una volta instauratasi, porti allo sviluppo del cancro.
I ceppi di HPV ad alto rischio (16, 18 ed altri) provocano il cancro della cervice; non si manifestano attraverso i condilomi, ma con modificazioni displasiche che possono evolvere in cancro.
L’integrazione del genoma HPV nella cellula ospite comporta la perdita del gene virale E2 che normalmente reprime l’espressione degli oncogeni E6 e E7 (che a loro volta stimolano la proliferazione cellulare) e la perdita della capacità di riparare i danni del DNA e di andare in apoptosi.
Diagnostica HPV: I mezzi diagnostici a disposizione per accertare la presenza di un’infezione HPV sono:
A) esame obiettivo:
- presenza di verruche o condilomi
- secrezioni vaginali abbondanti, che cambiano colore (da gialle a verdastre o grigie) e di odore sgradevole;
- dolore, di varia entità, o disagio nella zona pelvica o nell’addome inferiore. Il dolore può manifestarsi anche durante i rapporti sessuali (dispareunia);
- prurito o bruciore nell’area genitale;
- sanguinamento o spotting (sanguinamento leggero) intermestruale o fuori del periodo mestruale normale;
- aumento della frequenza urinaria.
- affaticamento, febbre lieve e malessere.
B) Thin-prep: Il grado di precisione diagnostica nell’esame citologico cervico-vaginale non è sufficiente per individuare tutti i casi di infezione (percentuale di falsi negativi non eliminabile del tutto).
C) Thin HPV DNA test (genotipizzazione virale): identificazione del DNA virale mediante PCR (Polymerase Chain Reaction) e ISH (in situ hybridization) indicata con il termine di PCR-ISH (3,4) che è in grado di combinare l’estrema sensibilità della PCR con la capacità di localizzazione topografica dell’ibridazione in situ. Il virus va ricercato sulle cellule raccolte con un normale striscio vaginale e della portio come per pap-test o meglio thin-prep ma il test di genotipizzazione virale può essere eseguito anche su campioni di sangue, urine e sperma. I campioni possono essere conservati fino a 24 ore in frigo a 4 °C oppure per lungo tempo a -80 °C.
ll Ministero della Salute ha inviato una nota a tutte le Regioni affermando che entrambi i test citologici sono utilizzabili per lo screening primario in donne che hanno compiuto i 30 anni. In presenza di un risultato negativo al test HPV utilizzato come screening primario, il controllo successivo viene effettuato dopo cinque anni e non dopo tre anni come succede dopo un Pap-test negativo. Il test HPV non è indicato per le donne con meno di 30 anni. Questo perché la maggior parte delle infezioni da HPV nella popolazione femminile si verifica all’inizio dell’attività sessuale, poi il sistema immunitario impara a riconoscere il virus e a reagire. Con un esame sensibile come il test HPV, la probabilità di trovare un’infezione in una donna giovane è molto alta, ma proprio queste donne vanno incontro facilmente alla risoluzione spontanea dell’infezione e delle lesioni. Sottoponendo al test le donne più giovani si rischia quindi di andare incontro a diagnosi scorrette e a eccessi di trattamento.
– DuoPap è un esame semplice, rapido e affidabile che unisce in un’unica ricerca le caratteristiche di due test (Ricerca HPV DNA e Pap Test) con lo scopo di prevenire il carcinoma della cervice uterina e rilevare eventuali alterazioni delle cellule del collo dell’utero.
– Full Pap è il test per la ricerca di RNA di HPV, in combinazione con la ricerca del DNA di HPV e la citologia in fase liquida (Pap test).
Colposcopia: E’ sempre opportuno, soprattutto in caso di ASCUS o LSIL, associare alla citologia la colposcopia e il controllo bioptico mirato delle lesioni sospette. Associando tali metodiche la quota di falsi negativi scende al di sotto del 5%.
Istologia: Per quanto riguarda i criteri morfologici di diagnosi istologica si fa riferimento alla classificazione CIN (Cervical Intraepithelial Neoplasia)/SIL.
Immuno-istochimica: Come ulteriore approfondimento è possibile richiedere l’analisi immunocitochimica di proteine P16 e KI-67 la cui espressione è marcatore di infezioni da HPV.
microscopia elettronica
Dunque, attualmente Ia diagnosi routinaria di infezione da HPV è affidata alla combinazione ispezione-citologia-colposcopia-biopsia. Utile associare l’esame di lembi endocervicali, prelevati mediante curettage del canale, laddove lo striscio citologico di donne affette da condiloma acuminato o piatto della portio e/o CIN, indichi anche la presenza di cellule ghiandolari atipiche. L’indagine può essere completata dall’effettuazione, in sede colposcopica, di una vulvoscopia, rivelatasi preziosa nel riscontro di lesioni subcliniche da HPV a livello vulvare.
Sebbene LSIL (comprendente infezione da HPV, displasia lieve, CIN1) sembra essere un’espressione benigna dell’infezione da papillomavirus, i fattori di rischio per lo sviluppo di questa lesione squamosa, sembrano essere distinti da quelli associati all’infezione da HPV, il che suggerisce che lo sviluppo della LSIL non corrisponda ad una semplice infezione da papillomavirus.
Recenti studi, effettuati su donne adulte, hanno dimostrato che una percentuale compresa tra il 20% ed il 40% per cento di queste LSIL, potevano evolvere verso lesioni di alto grado (HSIL, termine in cui sono compresi displasia moderata e grave, CIN2, CIN3 e Carcinoma in situ), con solo il 50-60% di regressione spontanea in relazione al grado di immunocompetenza individuale (19).
Non è più ritenuto valido il cytobrush endouretrale.
| Tab. 1 – Presidi diagnostici per HPV | ||||
|
Test |
Sensibilità |
Specificità |
Vantaggi |
Svantaggi |
|
Ispezione visiva |
– – – – |
+ + + + |
Semplice e rapida |
Identificazione delle |
|
Colposcopia/ Vulvoscopia |
+ + – – |
– – – – |
Identifica lesioni non |
Non tipizza l’HPV |
|
Tests sierologici |
– – – – |
– – – – |
Si può correlare con la progressione della malattia |
Inadatto per lo screening |
|
Citologia (Pap-test) |
– – – – |
+ + + + |
Poco costoso |
Non tipizza l’HPV |
|
Citologia (Thinprep) |
||||
|
Istologia |
||||
|
Test Hybrid capture |
+ + + + + + |
+ + + + + + |
Elevato costo |
|
| Tab. 2 – tests diagnostici molecolari per HPV | ||
| Test | Sensibilità | Specificità |
| Southern blot | +++ | +++ |
| Dot blot | + | +++ |
| Ibridizzazione in situ (ISH) | + | +++ |
| PCR-ISH Ibridizzazione in situ del DNA mediante PCR | ++++++ | +++ |
| Ibridizzazione in soluzione | +++ | +++ |
Recidive: La frequenza delle recidive è strettamente connessa con lo stato immunitario delle pazienti. La percentuale di recidive nella popolazione trattata per lesioni da HPV è di circa il 20%, tale percentuale sale al 65% se valutiamo un gruppo di pazienti immunocompromesse.
Esame colposcopico per il maschio: i 2/3 dei partners di pazienti HPV-positive sono portatori di infezione subclinica HPV. Si pratica esame penescopico e prelievo solo sulle zone di lesione più significative; Molte volte le lesioni si mettono in evidenza solo dopo trattamento con ac. acetico. Gli uomini con infezione sub-clinica rappresentano un serbatoio di riserva per reinfezioni successive alla terapia.
Questa pagina fa parte del sito fertilitycenter.it in internet da marzo 2011. I testi, le tabelle, i disegni e le immagini pubblicati in queste pagine sono coperte da copyright ma a disposizione di tutti per copia e riproduzione purchè venga citata la fonte con Link al sito www.fertilitycenter.it.
Ringrazio i lettori per la loro cortese attenzione e gradirei osservazioni e consigli su eventuali errori o esposizioni incomplete.
Enzo Volpicelli.
Bibliografia:
- Penna C, Fallani MG, Cariti G, Menichetti M, Bracco GL, Bellanti G, Cioffi M., Marchionni M.: “Utilizzo del methisoprinol (Viruxan) nella condilomatosi genitale femminile. Minerva Ginecol. 1989 Jan;41(1):27-32
- Krebs HB: “The use of topical 5-fluorouracil in the treatment of genital condylomas”. Obstet Gynecol Clin North Am. 1987 Jun; 14(2):559-68.
- Brown G.D., Gordon S.: Immune recognition of fungal Beta-glucans. Cell Microbiol. 2005;7(4):471-9. Review.
- Suram S et al.: Regulation q/ cytosolic phpspholipase A2 activation and cycloxygenase 2 expression in macrophages by the Beta-glucan receptor. J Biol Chem 2006;28 I (9):5506- 14
- Narisawa-Saito M., Kiyono T.: Basic mechanisms of high-risk human papillomavirus-induced carcinogenesis: Roles of E6 and E7proteins, Cancer Sci. 2007
- Penna C., Fallani M.G. et aL: Cervical intraepithelial neoplasia and genital condylomatosis in HIV-positive patients. Clinical aspects and management. Minerva Ginecol. l996;48(7-8):275-81.
- Smith M.C. et al.: A long-term study of women with normal colposcopy after referral with low-grade cytologicalabnormalities. BJOG. 2006; 113(11): 1321-8
SICPCV: Gestione della paziente con Pap-test anormale. Linee Guida Edizione 2006. Anno XXI;N.1 Dicembre 2006 - Pieralli A, Fallani MG, Penna C et al. L’azione immunomodulante del Beta-glucano come adiuvante nella regressione delle alterazioni citologiche cervicali di basso grado (ASCUS e LSIL). Ginecologia online 2007, Vol. 4.
- Warts Types, Causes, Symptoms, Treatments, Prevention”. Webmd.com. 2010-09-02. Retrieved 2013-05-17.
- Anderson, Keith,; Keith, Jeff; Novak, Patricia D.; Elliot, Michelle A. (2005). Mosby’s Medical, Nursing, and Allied Health Dictionary (5th ed.). C.V. Mosby.
- de Villiers EM, Fauquet C, Broker TR, Bernard HU, zur Hausen H (Jun 2004). “Classification of papillomaviruses”. Virology 324 (1): 17–27.
- Wang H, Qiao YL.: “Human papillomavirus type-distribution in condylomata acuminata of mainland China: a meta-analysis”. Int J STD AIDS. 2008 Oct; 19(10):680-4.
- Hsueh PR.: “Human papillomavirus, genital warts, and vaccines”. J Microbiol Immunol Infect. 2009 Apr; 42(2):101-6.
- Perno C.F., Svicher V., Ceccherini-Silberstein F., Ciotti m.: “Il papillomavirus umano e il cancro della cervice uterina: epidemiologia, basi genetiche e prevenzione”. It J Gynecol Obstet. 2007,19:4:198-207.
- Papillomavirus, eMedicine, 2007. URL consultato il 16 agosto 2009.
- Muñoza N, Castellsaguéb X, Berrington de Gonzálezc A, Gissmann L, Chapter 1: HPV in the etiology of human cancer in Vaccine, vol. 24, nº 3, 2006, pp. S1–S10.
- HUMAN PAPILLOMAVIRUSES HPV types 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 and 66 (Group 1) – HPV 6 and HPV 11 (Group 2B), IARC, 2006.
- Vaccination to prevent and treat cervical cancer Hum Pathol. 2004 Aug;35(8):971
- Anna.-Barbara Moscicki et al. Regression of low-grade squamous intra-epithelial lesions in young women. Lancet 2004; 364:1678-83
- Sherr C, Principles of tumor suppression in Cell, vol. 116, nº 2, 2004, pp. 235–46
- LOUISE T. CHOW, THOMAS R. BROKER and BETTIE M. STEINBERG: “The natural history of human papillomavirus infections of the mucosal epithelia”. Journal Compilation 2010 APMIS